రచయిత:
Monica Porter
సృష్టి తేదీ:
17 మార్చి 2021
నవీకరణ తేదీ:
1 జూలై 2024

విషయము
మోలార్ ఏకాగ్రత ఒక ద్రావకం యొక్క మోల్స్ సంఖ్య మరియు ద్రావణం యొక్క వాల్యూమ్ మధ్య సంబంధాన్ని సూచిస్తుంది. మొలారిటీని లెక్కించడానికి, మీరు మోల్స్ మరియు వాల్యూమ్, ద్రవ్యరాశి మరియు వాల్యూమ్ లేదా మోల్స్ మరియు మిల్లీలీటర్లతో (మి.లీ) ప్రారంభించవచ్చు. అప్పుడు, పై వేరియబుల్స్తో, సరైన ఫలితాన్ని పొందడానికి ప్రాథమిక మోలార్ ఏకాగ్రత సూత్రాన్ని వర్తించండి.
దశలు
4 యొక్క పద్ధతి 1: మోలార్ సంఖ్య మరియు వాల్యూమ్ నుండి మోల్ ఏకాగ్రతను లెక్కించండి
మోలార్ ఏకాగ్రతను లెక్కించడానికి ప్రాథమిక సూత్రాన్ని తెలుసుకోవడం చాలా ముఖ్యం. మోలార్ గా ration త ఒక ద్రావకం యొక్క మోల్స్ సంఖ్యకు సమానం, ద్రావణం యొక్క వాల్యూమ్ ద్వారా లీటర్లలో విభజించబడింది. అక్కడ నుండి, మనకు ఈ క్రింది సూత్రం ఉంది: మోలార్ ఏకాగ్రత = ద్రావణం యొక్క మోల్స్ సంఖ్య / లీటరు ద్రావణం సంఖ్య
- ఉదాహరణ: 4.2 లీటర్ల ద్రావణంలో NaCl యొక్క 0.75 మోల్స్ కలిగిన ద్రావణం యొక్క మోలార్ గా ration త ఎంత?

అంశాన్ని విశ్లేషించండి. మోలార్ గా ration తను లెక్కించడానికి, మీకు మోల్స్ సంఖ్య మరియు లీటర్లలో ద్రావణం యొక్క పరిమాణం అవసరం. ఇచ్చిన అంశం కారణంగా మీరు ఈ రెండు విలువలను లెక్కించాల్సిన అవసరం లేదు.- ఉదాహరణకి:
- మోల్స్ సంఖ్య = NaCl యొక్క 0.75 మోల్స్
- వాల్యూమ్ = 4.2 ఎల్
- ఉదాహరణకి:
మోల్స్ సంఖ్యను వాల్యూమ్ ద్వారా విభజించండి. వాల్యూమ్ ద్వారా మోల్ విభజన యొక్క ఫలితం లీటరు ద్రావణానికి మోల్స్ సంఖ్య లేదా ఆ ద్రావణం యొక్క మోలార్ గా ration త.
- ఉదాహరణ: మోలార్ ఏకాగ్రత = ద్రావణం యొక్క మోల్స్ సంఖ్య / ద్రావణ లీటర్ల సంఖ్య = 0.75 మోల్ / 4.2 ఎల్ = 0.17857142

మీ ఫలితాలను రికార్డ్ చేయండి. ఉపాధ్యాయుడి అభ్యర్థన లేదా అసైన్మెంట్ను బట్టి కామా తర్వాత రెండు లేదా మూడు సంఖ్యలకు రౌండ్ చేయండి. మీ ఫలితాలను రికార్డ్ చేసేటప్పుడు, "మోలార్ గా ration త" ను "M" తో సంక్షిప్తీకరించండి మరియు ద్రావకం యొక్క రసాయన చిహ్నాన్ని చేర్చండి.- ఉదాహరణకి: 0.179 ఓం NaCl
4 యొక్క పద్ధతి 2: మాస్ మరియు వాల్యూమ్ నుండి మోల్ ఏకాగ్రతను లెక్కించండి
మోలార్ ఏకాగ్రతను లెక్కించడానికి ప్రాథమిక సూత్రాన్ని అర్థం చేసుకోవడం అవసరం. మోలార్ ఏకాగ్రత ఒక ద్రావకం యొక్క మోల్స్ సంఖ్య మరియు ద్రావణం యొక్క వాల్యూమ్ మధ్య సంబంధాన్ని చూపుతుంది. మోలార్ ఏకాగ్రత యొక్క సూత్రం క్రింది విధంగా ఉంది: మోలార్ ఏకాగ్రత = ద్రావణ ఏకాగ్రత / లీటరు ద్రావణం సంఖ్య
- సమస్య ఉదాహరణ: 3,4 గ్రాముల KMnO ను కరిగించిన తరువాత ద్రావణం యొక్క మోల్స్ సంఖ్యను లెక్కించండి4 5.2 లీటర్ల నీటిలో.

అంశాన్ని విశ్లేషించండి: మోలార్ ఏకాగ్రతను కనుగొనడానికి, మీకు మోల్స్ సంఖ్య మరియు లీటర్లలో ద్రావణం యొక్క పరిమాణం అవసరం. ఈ విలువలు ఇవ్వకపోతే, కానీ ద్రావణం యొక్క వాల్యూమ్ మరియు ద్రవ్యరాశి మీకు తెలిస్తే, మోలార్ ఏకాగ్రతను లెక్కించే ముందు మీరు ద్రావణం యొక్క మోల్స్ సంఖ్యను నిర్ణయించవచ్చు.- ఉదాహరణకి:
- బరువు = 3.4 గ్రా KMnO4
- వాల్యూమ్ = 5.2 ఎల్
- ఉదాహరణకి:
ద్రావకం యొక్క ద్రవ్యరాశి అణువును లెక్కించండి. ఆ ద్రవ్యరాశి లేదా గ్రాముల ద్రావణం నుండి ద్రావణం యొక్క మోల్స్ సంఖ్యను లెక్కించడానికి, మీరు మొదట ద్రావకం యొక్క ద్రవ్యరాశి అణువును నిర్ణయించాలి. ద్రావణంలో ప్రతి మూలకం యొక్క ద్రవ్యరాశి అణువును జోడించడం ద్వారా ద్రావకం యొక్క ద్రవ్యరాశి అణువును నిర్ణయించవచ్చు. ప్రతి మూలకం యొక్క క్యూబిక్ అణువును కనుగొనడానికి, మూలకాల యొక్క ఆవర్తన పట్టికను ఉపయోగించండి.
- ఉదాహరణకి:
- K యొక్క మాస్ అణువు = 39.1 గ్రా
- Mn యొక్క ద్రవ్యరాశి అణువు = 54,9 గ్రా
- O = 16,0 గ్రా మాస్ అణువు
- ద్రవ్యరాశి యొక్క మొత్తం అణువుల = K + Mn + O + O + O + O = 39.1 + 54.9 + 16 + 16 + 16 + 16 = 158.0 గ్రా
- ఉదాహరణకి:
గ్రాములను మోల్స్గా మార్చండి. మీరు ఒక క్యూబిక్ అణువును కలిగి ఉంటే, మీరు ద్రావణంలో ఒక మోలార్ ద్రవ్యరాశికి 1 మోల్ సమానమైన మార్పిడి కారకం ద్వారా ద్రావణంలో గ్రాముల గ్రాముల సంఖ్యను గుణించాలి. ఈ గుణకారం యొక్క ఫలితం ద్రావకం యొక్క మోల్స్ సంఖ్య.
- ఉదాహరణ: గ్రాముల ద్రావణం * (1 / మోలార్ ద్రవ్యరాశి) = 3.4 గ్రా * (1 మోల్ / 158 గ్రా) = 0.0215 మోల్
మోల్స్ సంఖ్యను లీటర్ల సంఖ్యతో విభజించండి. ఇప్పుడు మీరు మోల్స్ సంఖ్యను లెక్కించారు, ఇప్పుడు ఆ సంఖ్యను ద్రావణం యొక్క వాల్యూమ్ ద్వారా లీటర్లలో విభజించండి, మీకు ఆ ద్రావణం యొక్క మోలార్ గా ration త ఉంటుంది.
- ఉదాహరణ: మోలార్ ఏకాగ్రత = ద్రావణ మోల్స్ సంఖ్య / లీటరు ద్రావణం సంఖ్య = 0.0215 మోల్ / 5.2 ఎల్ = 0.004134615
మీ ఫలితాలను రికార్డ్ చేయండి. ఉపాధ్యాయుడికి అవసరమైన విధంగా మీరు ఫలితాలను చుట్టుముట్టాలి, సాధారణంగా కామా తర్వాత రెండు నుండి మూడు సంఖ్యలు. అదనంగా, ఫలితాన్ని వ్రాసేటప్పుడు, "మోలార్ గా ration త" ను "M" అని సంక్షిప్తీకరించండి మరియు ద్రావణం యొక్క రసాయన చిహ్నంతో పాటు.
- ఉదాహరణకి: 0.004 M KMnO4
4 యొక్క విధానం 3: మోల్స్ మరియు ద్రావణం యొక్క మిల్లీలీటర్ల సంఖ్య నుండి మోలార్ గా ration తను లెక్కించండి
మోలార్ ఏకాగ్రత కోసం సూత్రాన్ని తెలుసుకోవాలి. మోలార్ ఏకాగ్రతను లెక్కించడానికి. మీరు ఒక లీటరు ద్రావణానికి ద్రావణం యొక్క మోల్స్ సంఖ్యను లెక్కించాలి, ద్రావణం యొక్క మిల్లీలీటర్ కాదు. మోలార్ గా ration తను లెక్కించడానికి సాధారణ సూత్రం: మోలార్ ఏకాగ్రత = ద్రావణం యొక్క మోల్స్ సంఖ్య / లీటరు ద్రావణం సంఖ్య
- ఉదాహరణ: CaCl యొక్క 1.2 మోల్స్ కలిగిన ద్రావణం యొక్క మోలార్ గా ration తను లెక్కించండి2 2905 మిల్లీలీటర్ల నీటిలో.
అంశాన్ని విశ్లేషించండి. మోలార్ గా ration తను లెక్కించడానికి, మీకు ద్రావకం యొక్క మోల్స్ సంఖ్య మరియు లీటర్లలో ద్రావణం యొక్క పరిమాణం అవసరం. మిల్లీలీటర్లలో సమస్యలో ద్రావణం యొక్క వాల్యూమ్ ఇవ్వబడితే, లెక్కింపు చేయడానికి ముందు లీటర్లలో సమానమైన వాల్యూమ్కు మార్చండి.
- ఉదాహరణకి:
- మోల్స్ సంఖ్య = CaCl యొక్క 1.2 మోల్స్2
- వాల్యూమ్ = 2905 మి.లీ.
- ఉదాహరణకి:
మిల్లీలీటర్లను లీటర్లకు మార్చండి. ద్రావణాన్ని మిల్లీలీటర్ల నుండి లీటర్లకు మార్చడానికి, మిల్లీలీటర్ల సంఖ్యను 1000 ద్వారా విభజించండి, ఎందుకంటే ప్రతి లీటరు 1000 మిల్లీలీటర్లకు సమానం. మిగిలి ఉన్న దశాంశ బిందువు 3 అంకెలను మార్చడం ద్వారా మీరు మిల్లీలీటర్లను లీటర్లకు మార్చవచ్చు.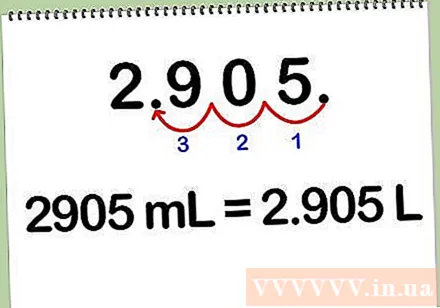
- ఉదాహరణకు: 2905 ml * (1 L / 1000 ml) = 2,905 L.
మోల్స్ సంఖ్యను లీటర్ల సంఖ్యతో విభజించండి. మీరు లీటర్ల సంఖ్యను కలిగి ఉన్న తరువాత, మోల్ సంఖ్యను లీటర్ల ద్రావణాల సంఖ్యతో విభజించడం ద్వారా మీరు మోలార్ గా ration తను లెక్కించవచ్చు.
- ఉదాహరణ: మోలార్ ఏకాగ్రత = ద్రావణం యొక్క మోల్స్ సంఖ్య / లీటరు ద్రావణం సంఖ్య = 1.2 మోల్స్ CaCl2 / 2,905 ఎల్ = 0.413080895
మీ ఫలితాలను రికార్డ్ చేయండి. ఫలితాన్ని రెండు లేదా మూడు కామాలతో లేదా మీ గురువు కోరినట్లు గుర్తుంచుకోండి. ఫలితాన్ని రికార్డ్ చేసేటప్పుడు, "మోలార్ గా ration త" ను "M" అని సంక్షిప్తీకరించండి మరియు తరువాత ద్రావణానికి రసాయన చిహ్నం.
- ఉదాహరణకి: 0.413 M CaCl2
4 యొక్క విధానం 4: అదనపు ప్రాక్టీస్
5.2 గ్రా NaCl 800 మి.లీ నీటిలో కరిగినప్పుడు ఒక పరిష్కారం యొక్క మోలార్ గా ration తను లెక్కించండి. సమస్య ఇచ్చిన విలువలను నిర్ణయించండి: గ్రాములలో ద్రవ్యరాశి మరియు మిల్లీలీటర్లలో వాల్యూమ్.
- మాస్ = 5.2 గ్రా NaCl
- వాల్యూమ్ = 800 మి.లీ నీరు
Na మూలకం యొక్క క్యూబిక్ అణువును మరియు Cl యొక్క క్యూబిక్ అణువును జోడించడం ద్వారా NaCl యొక్క ద్రవ్యరాశి అణువును కనుగొనండి.
- Na = 22.99 గ్రా ద్రవ్యరాశి అణువు
- Cl = 35.45 గ్రా మాస్ అణువు
- NaCl = 22.99 + 35.45 = 58.44 గ్రా యొక్క ద్రవ్యరాశి అణువులు
మోలార్ మార్పిడి కారకం ద్వారా ద్రావకం యొక్క ద్రవ్యరాశిని గుణించండి. ఈ ఉదాహరణలో, NaCl యొక్క పరమాణు ద్రవ్యరాశి 58.44 గ్రా, కాబట్టి మార్పిడి కారకం “1 మోల్ / 58.44 గ్రా”.
- NaCl మోల్ సంఖ్య = 5.2 గ్రా NaCl * (1 mol / 58.44 g) = 0.8898 mol = 0.09 mol
800 మి.లీ నీటిని 1000 ద్వారా విభజించండి, మీరు లీటర్లలో నీటి పరిమాణాన్ని పొందుతారు.
- మీరు మిల్లీలీటర్ నుండి లీటరు వరకు 1 ఎల్ / 1000 మి.లీ మార్పిడి కారకం ద్వారా 800 మి.లీ గుణించవచ్చు.
- గుణకారం ప్రక్రియను పైన పేర్కొన్న విధంగా తగ్గించడానికి, మీరు దశాంశ బిందువు 3 అంకెలను ఎడమ వైపుకు బ్యాక్ చేయవచ్చు.
- వాల్యూమ్ = 800 మి.లీ * (1 ఎల్ / 1000 మి.లీ) = 800 మి.లీ / 1000 మి.లీ = 0.8 ఎల్
లీటర్లలో ద్రావణం యొక్క వాల్యూమ్ ద్వారా ద్రావణం యొక్క మోల్స్ సంఖ్యను విభజించండి. మోలార్ ఏకాగ్రతను లెక్కించడానికి, మీరు 0.09 మోల్స్ ద్రావణాన్ని (ఈ సందర్భంలో, NaCl) లీటర్లలో ద్రావణం యొక్క వాల్యూమ్ ద్వారా విభజించాలి.
- మోలార్ ఏకాగ్రత = ద్రావణం యొక్క మోల్స్ సంఖ్య / ద్రావణం లీటర్ల సంఖ్య = 0.09 మోల్ / 0.8 ఎల్ = 0.1125 మోల్ / ఎల్
తుది ఫలితాన్ని రికార్డ్ చేయండి. కామా తర్వాత ఫలితాన్ని రెండు లేదా మూడు సంఖ్యలకు రౌండ్ చేయండి మరియు ద్రావణ రసాయన చిహ్నంతో కలిసి "M" తో "మోలార్ గా ration త" ను సంక్షిప్తీకరించండి.
- ఫలితం: 0.11 M NaCl