రచయిత:
Eric Farmer
సృష్టి తేదీ:
10 మార్చి 2021
నవీకరణ తేదీ:
1 జూలై 2024

విషయము
- దశలు
- 2 వ పద్ధతి 1: అణువులలో న్యూట్రాన్ల సంఖ్యను నిర్ణయించడం (ఐసోటోపులు కాదు)
- 2 వ పద్ధతి 2: ఐసోటోపులలోని న్యూట్రాన్ల సంఖ్యను నిర్ణయించడం
- చిట్కాలు
ఒకే మూలకం యొక్క అణువులలో, ప్రోటాన్ల సంఖ్య స్థిరంగా ఉంటుంది, న్యూట్రాన్ల సంఖ్య మారవచ్చు.ఒక నిర్దిష్ట అణువు ఎన్ని న్యూట్రాన్లను కలిగి ఉందో తెలుసుకోవడం ద్వారా, ఇది సాధారణ అణువునా లేదా తక్కువ లేదా ఎక్కువ న్యూట్రాన్లను కలిగి ఉండే ఐసోటోప్ కాదా అని మీరు నిర్ణయించవచ్చు. అణువులోని న్యూట్రాన్ల సంఖ్యను నిర్ణయించడం చాలా సులభం. ఒక అణువు లేదా ఐసోటోప్లోని న్యూట్రాన్ల సంఖ్యను లెక్కించడానికి మీరు చేయాల్సిందల్లా మా సూచనలను పాటించడం మరియు ఆవర్తన పట్టికను సులభంగా ఉంచడం.
దశలు
2 వ పద్ధతి 1: అణువులలో న్యూట్రాన్ల సంఖ్యను నిర్ణయించడం (ఐసోటోపులు కాదు)
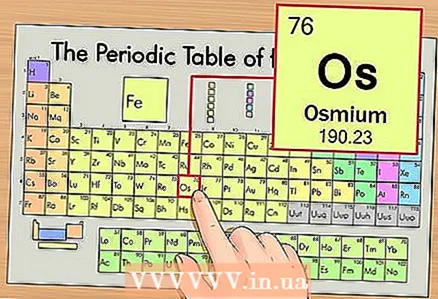 1 ఆవర్తన పట్టికలో మూలకాన్ని కనుగొనండి. ఉదాహరణగా, మేము ఆరవ కాలంలో (ఎగువ నుండి ఆరవ వరుస) ఉన్న ఓస్మియం (ఓస్) ను పరిశీలిస్తాము.
1 ఆవర్తన పట్టికలో మూలకాన్ని కనుగొనండి. ఉదాహరణగా, మేము ఆరవ కాలంలో (ఎగువ నుండి ఆరవ వరుస) ఉన్న ఓస్మియం (ఓస్) ను పరిశీలిస్తాము.  2 మూలకం యొక్క పరమాణు సంఖ్యను కనుగొనండి. ఇది ఒక నియమం వలె, ఒక మూలకం యొక్క సెల్లో గుర్తించదగిన సంఖ్య మరియు సాధారణంగా దాని గుర్తు పైన ఉంటుంది (మా ఉదాహరణలో మనం ఉపయోగించే ఆవర్తన పట్టిక యొక్క సంస్కరణలో, ఇతర సంఖ్యలు లేవు). పరమాణు సంఖ్య అంటే ఆ మూలకం యొక్క ఒక అణువులోని ప్రోటాన్ల సంఖ్య. ఓస్మియం కొరకు, ఈ సంఖ్య 76, అంటే, ఒక ఓస్మియం అణువులో 76 ప్రోటాన్లు ఉంటాయి.
2 మూలకం యొక్క పరమాణు సంఖ్యను కనుగొనండి. ఇది ఒక నియమం వలె, ఒక మూలకం యొక్క సెల్లో గుర్తించదగిన సంఖ్య మరియు సాధారణంగా దాని గుర్తు పైన ఉంటుంది (మా ఉదాహరణలో మనం ఉపయోగించే ఆవర్తన పట్టిక యొక్క సంస్కరణలో, ఇతర సంఖ్యలు లేవు). పరమాణు సంఖ్య అంటే ఆ మూలకం యొక్క ఒక అణువులోని ప్రోటాన్ల సంఖ్య. ఓస్మియం కొరకు, ఈ సంఖ్య 76, అంటే, ఒక ఓస్మియం అణువులో 76 ప్రోటాన్లు ఉంటాయి. - ప్రోటాన్ల సంఖ్య మారదు మరియు ఇది ఒక మూలకాన్ని ఒక మూలకం చేస్తుంది.
 3 ఒక మూలకం యొక్క పరమాణు ద్రవ్యరాశిని కనుగొనండి. ఈ సంఖ్య సాధారణంగా మూలకం చిహ్నం క్రింద కనిపిస్తుంది. దయచేసి మా ఉదాహరణలోని ఆవర్తన పట్టిక యొక్క సంస్కరణలో, పరమాణు ద్రవ్యరాశి ఇవ్వబడలేదు (ఇది ఎల్లప్పుడూ అలా కాదు; ఆవర్తన పట్టిక యొక్క అనేక వెర్షన్లలో, పరమాణు ద్రవ్యరాశి సూచించబడుతుంది). ఓస్మియం యొక్క పరమాణు ద్రవ్యరాశి 190.23.
3 ఒక మూలకం యొక్క పరమాణు ద్రవ్యరాశిని కనుగొనండి. ఈ సంఖ్య సాధారణంగా మూలకం చిహ్నం క్రింద కనిపిస్తుంది. దయచేసి మా ఉదాహరణలోని ఆవర్తన పట్టిక యొక్క సంస్కరణలో, పరమాణు ద్రవ్యరాశి ఇవ్వబడలేదు (ఇది ఎల్లప్పుడూ అలా కాదు; ఆవర్తన పట్టిక యొక్క అనేక వెర్షన్లలో, పరమాణు ద్రవ్యరాశి సూచించబడుతుంది). ఓస్మియం యొక్క పరమాణు ద్రవ్యరాశి 190.23.  4 పరమాణు ద్రవ్యరాశిని సమీప మొత్తం సంఖ్యకు రౌండ్ చేయండి. మా ఉదాహరణలో, 190.23 190 కి గుండ్రంగా ఉంటుంది.
4 పరమాణు ద్రవ్యరాశిని సమీప మొత్తం సంఖ్యకు రౌండ్ చేయండి. మా ఉదాహరణలో, 190.23 190 కి గుండ్రంగా ఉంటుంది. - పరమాణు ద్రవ్యరాశి అనేది ఒక నిర్దిష్ట మూలకం యొక్క సగటు ఐసోటోపుల సంఖ్య, సాధారణంగా ఇది పూర్ణాంకంగా వ్యక్తీకరించబడదు.
 5 పరమాణు ద్రవ్యరాశి నుండి పరమాణు సంఖ్యను తీసివేయండి. ప్రోటాన్లు మరియు న్యూట్రాన్లు పరమాణు ద్రవ్యరాశి యొక్క సంపూర్ణ భాగాన్ని కలిగి ఉన్నందున, పరమాణు ద్రవ్యరాశి నుండి ప్రోటాన్ల సంఖ్యను (అంటే ప్రోటాన్ల సంఖ్యతో సమానమైన పరమాణు సంఖ్యను తీసివేయడం) అణువులోని న్యూట్రాన్ల సంఖ్యను ఇస్తుంది. దశాంశ బిందువు తర్వాత ఉన్న సంఖ్యలు పరమాణువులోని అతి తక్కువ ఎలక్ట్రాన్ల ద్రవ్యరాశిని సూచిస్తాయి. మా ఉదాహరణలో: 190 (పరమాణు బరువు) - 76 (ప్రోటాన్ల సంఖ్య) = 114 (న్యూట్రాన్ల సంఖ్య).
5 పరమాణు ద్రవ్యరాశి నుండి పరమాణు సంఖ్యను తీసివేయండి. ప్రోటాన్లు మరియు న్యూట్రాన్లు పరమాణు ద్రవ్యరాశి యొక్క సంపూర్ణ భాగాన్ని కలిగి ఉన్నందున, పరమాణు ద్రవ్యరాశి నుండి ప్రోటాన్ల సంఖ్యను (అంటే ప్రోటాన్ల సంఖ్యతో సమానమైన పరమాణు సంఖ్యను తీసివేయడం) అణువులోని న్యూట్రాన్ల సంఖ్యను ఇస్తుంది. దశాంశ బిందువు తర్వాత ఉన్న సంఖ్యలు పరమాణువులోని అతి తక్కువ ఎలక్ట్రాన్ల ద్రవ్యరాశిని సూచిస్తాయి. మా ఉదాహరణలో: 190 (పరమాణు బరువు) - 76 (ప్రోటాన్ల సంఖ్య) = 114 (న్యూట్రాన్ల సంఖ్య). 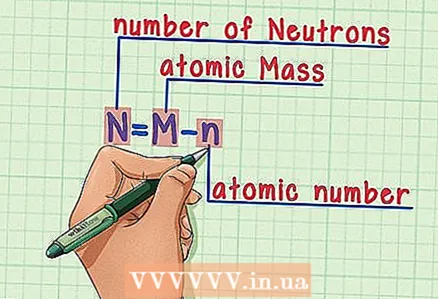 6 సూత్రాన్ని గుర్తుంచుకోండి. భవిష్యత్తులో న్యూట్రాన్ల సంఖ్యను కనుగొనడానికి, ఈ సూత్రాన్ని ఉపయోగించండి:
6 సూత్రాన్ని గుర్తుంచుకోండి. భవిష్యత్తులో న్యూట్రాన్ల సంఖ్యను కనుగొనడానికి, ఈ సూత్రాన్ని ఉపయోగించండి: - N = M - n
- N = న్యూట్రాన్ల సంఖ్య
- M = పరమాణు ద్రవ్యరాశి
- n = పరమాణు సంఖ్య
- N = M - n
2 వ పద్ధతి 2: ఐసోటోపులలోని న్యూట్రాన్ల సంఖ్యను నిర్ణయించడం
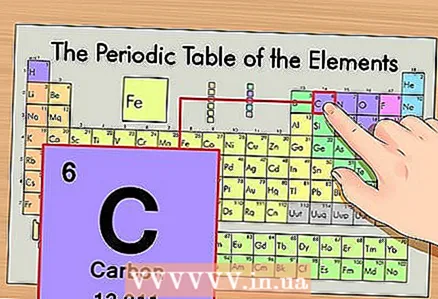 1 ఆవర్తన పట్టికలో మూలకాన్ని కనుగొనండి. ఉదాహరణగా, మేము కార్బన్ 14C ఐసోటోప్ను పరిశీలిస్తాము. నాన్-ఐసోటోపిక్ కార్బన్ 14C కేవలం కార్బన్ C కనుక, ఆవర్తన పట్టికలో కార్బన్ను కనుగొనండి (పై నుండి రెండవ కాలం లేదా రెండవ వరుస).
1 ఆవర్తన పట్టికలో మూలకాన్ని కనుగొనండి. ఉదాహరణగా, మేము కార్బన్ 14C ఐసోటోప్ను పరిశీలిస్తాము. నాన్-ఐసోటోపిక్ కార్బన్ 14C కేవలం కార్బన్ C కనుక, ఆవర్తన పట్టికలో కార్బన్ను కనుగొనండి (పై నుండి రెండవ కాలం లేదా రెండవ వరుస). 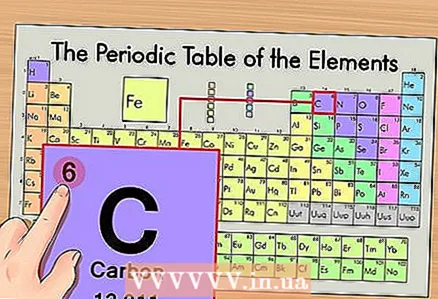 2 మూలకం యొక్క పరమాణు సంఖ్యను కనుగొనండి. ఇది ఒక నియమం వలె, ఒక మూలకం యొక్క సెల్లో గుర్తించదగిన సంఖ్య మరియు సాధారణంగా దాని గుర్తు పైన ఉంటుంది (మా ఉదాహరణలో మనం ఉపయోగించే ఆవర్తన పట్టిక యొక్క సంస్కరణలో, ఇతర సంఖ్యలు లేవు). పరమాణు సంఖ్య అంటే ఆ మూలకం యొక్క ఒక అణువులోని ప్రోటాన్ల సంఖ్య. కార్బన్ సంఖ్య 6, అంటే ఒక కార్బన్ ఆరు ప్రోటాన్లను కలిగి ఉంటుంది.
2 మూలకం యొక్క పరమాణు సంఖ్యను కనుగొనండి. ఇది ఒక నియమం వలె, ఒక మూలకం యొక్క సెల్లో గుర్తించదగిన సంఖ్య మరియు సాధారణంగా దాని గుర్తు పైన ఉంటుంది (మా ఉదాహరణలో మనం ఉపయోగించే ఆవర్తన పట్టిక యొక్క సంస్కరణలో, ఇతర సంఖ్యలు లేవు). పరమాణు సంఖ్య అంటే ఆ మూలకం యొక్క ఒక అణువులోని ప్రోటాన్ల సంఖ్య. కార్బన్ సంఖ్య 6, అంటే ఒక కార్బన్ ఆరు ప్రోటాన్లను కలిగి ఉంటుంది. 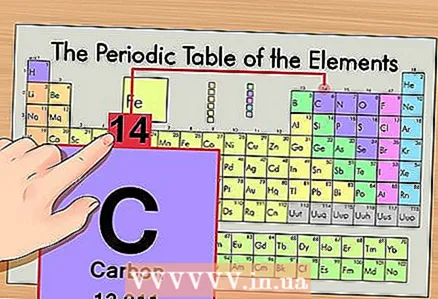 3 పరమాణు ద్రవ్యరాశిని కనుగొనండి. ఐసోటోపుల విషయంలో, దీన్ని చేయడం చాలా సులభం, ఎందుకంటే వాటికి వాటి పరమాణు ద్రవ్యరాశి ప్రకారం పేరు పెట్టారు. మా విషయంలో, కార్బన్ 14C 14 యొక్క పరమాణు ద్రవ్యరాశిని కలిగి ఉంది. ఇప్పుడు ఐసోటోప్ యొక్క పరమాణు ద్రవ్యరాశి మనకు తెలుసు; తదుపరి గణన ప్రక్రియ అణువులలోని న్యూట్రాన్ల సంఖ్యను నిర్ణయించడానికి సమానంగా ఉంటుంది (ఐసోటోపులు కాదు).
3 పరమాణు ద్రవ్యరాశిని కనుగొనండి. ఐసోటోపుల విషయంలో, దీన్ని చేయడం చాలా సులభం, ఎందుకంటే వాటికి వాటి పరమాణు ద్రవ్యరాశి ప్రకారం పేరు పెట్టారు. మా విషయంలో, కార్బన్ 14C 14 యొక్క పరమాణు ద్రవ్యరాశిని కలిగి ఉంది. ఇప్పుడు ఐసోటోప్ యొక్క పరమాణు ద్రవ్యరాశి మనకు తెలుసు; తదుపరి గణన ప్రక్రియ అణువులలోని న్యూట్రాన్ల సంఖ్యను నిర్ణయించడానికి సమానంగా ఉంటుంది (ఐసోటోపులు కాదు).  4 పరమాణు ద్రవ్యరాశి నుండి పరమాణు సంఖ్యను తీసివేయండి. ప్రోటాన్లు మరియు న్యూట్రాన్లు పరమాణు ద్రవ్యరాశి యొక్క సంపూర్ణ భాగాన్ని కలిగి ఉన్నందున, పరమాణు ద్రవ్యరాశి నుండి ప్రోటాన్ల సంఖ్యను (అంటే ప్రోటాన్ల సంఖ్యతో సమానమైన పరమాణు సంఖ్యను తీసివేయడం) అణువులోని న్యూట్రాన్ల సంఖ్యను ఇస్తుంది. మా ఉదాహరణలో: 14 (పరమాణు ద్రవ్యరాశి) - 6 (ప్రోటాన్ల సంఖ్య) = 8 (న్యూట్రాన్ల సంఖ్య).
4 పరమాణు ద్రవ్యరాశి నుండి పరమాణు సంఖ్యను తీసివేయండి. ప్రోటాన్లు మరియు న్యూట్రాన్లు పరమాణు ద్రవ్యరాశి యొక్క సంపూర్ణ భాగాన్ని కలిగి ఉన్నందున, పరమాణు ద్రవ్యరాశి నుండి ప్రోటాన్ల సంఖ్యను (అంటే ప్రోటాన్ల సంఖ్యతో సమానమైన పరమాణు సంఖ్యను తీసివేయడం) అణువులోని న్యూట్రాన్ల సంఖ్యను ఇస్తుంది. మా ఉదాహరణలో: 14 (పరమాణు ద్రవ్యరాశి) - 6 (ప్రోటాన్ల సంఖ్య) = 8 (న్యూట్రాన్ల సంఖ్య). 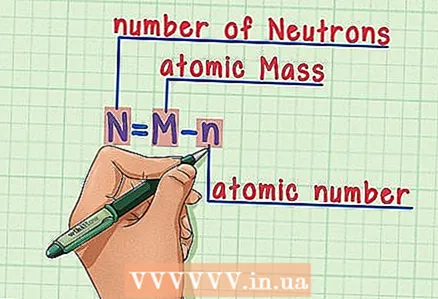 5 సూత్రాన్ని గుర్తుంచుకోండి. భవిష్యత్తులో న్యూట్రాన్ల సంఖ్యను కనుగొనడానికి, ఈ సూత్రాన్ని ఉపయోగించండి:
5 సూత్రాన్ని గుర్తుంచుకోండి. భవిష్యత్తులో న్యూట్రాన్ల సంఖ్యను కనుగొనడానికి, ఈ సూత్రాన్ని ఉపయోగించండి: - N = M - n
- N = న్యూట్రాన్ల సంఖ్య
- M = పరమాణు ద్రవ్యరాశి
- n = పరమాణు సంఖ్య
- N = M - n
చిట్కాలు
- ప్రోటాన్లు మరియు న్యూట్రాన్లు దాదాపు సంపూర్ణ మూలకాల ద్రవ్యరాశిని తయారు చేస్తాయి, అయితే ఎలక్ట్రాన్లు మరియు ఇతర కణాలు చాలా తక్కువ ద్రవ్యరాశిని కలిగి ఉంటాయి (ఈ ద్రవ్యరాశి సున్నాకి ఉంటుంది).ఒక ప్రోటాన్ ఒక న్యూట్రాన్తో సమానమైన ద్రవ్యరాశిని కలిగి ఉంటుంది మరియు పరమాణు సంఖ్య ప్రోటాన్ల సంఖ్య కాబట్టి, మీరు మొత్తం ద్రవ్యరాశి నుండి ప్రోటాన్ల సంఖ్యను తీసివేయవచ్చు.
- ఓస్మియం - గది ఉష్ణోగ్రత వద్ద ఘన స్థితిలో ఉన్న లోహం, గ్రీకు పదం "ఓస్మే" నుండి దాని పేరు వచ్చింది - వాసన.
- ఆవర్తన పట్టికలోని సంఖ్య అంటే ఏమిటో మీకు తెలియకపోతే, గుర్తుంచుకోండి: పట్టిక సాధారణంగా ఒక పరమాణు సంఖ్య (అంటే ప్రోటాన్ల సంఖ్య) చుట్టూ నిర్మించబడుతుంది, ఇది 1 (హైడ్రోజన్) వద్ద మొదలై ఒక యూనిట్ను ఎడమ నుండి కుడికి పెంచుతుంది , 118 (ఒగనెస్సన్) తో ముగుస్తుంది. ఎందుకంటే పరమాణువులోని ప్రోటాన్ల సంఖ్య మూలకాన్ని నిర్ణయిస్తుంది, మరియు అలాంటి సంఖ్య మూలకాలను నిర్వహించడానికి సులభమైన మార్గం (ఉదాహరణకు, 2 ప్రోటాన్లతో ఉండే పరమాణువు ఎల్లప్పుడూ హీలియం, 79 ప్రోటాన్లతో ఉండే పరమాణువు ఎల్లప్పుడూ బంగారంగా ఉంటుంది ).