రచయిత:
Lewis Jackson
సృష్టి తేదీ:
6 మే 2021
నవీకరణ తేదీ:
1 జూలై 2024

విషయము
సగటు ద్రవ్యరాశి అణువు అణువు యొక్క ద్రవ్యరాశి యొక్క ప్రత్యక్ష కొలత కాదు. బదులుగా, ఇది మూలకం యొక్క సాధారణ నమూనా నుండి అణువుకు సగటు ద్రవ్యరాశి. మీరు బిలియన్ల వ్యక్తిగత అణువుల ద్రవ్యరాశిని కొలవగలిగితే, వాటి సగటును లెక్కించడం ద్వారా మీరు దీన్ని కనుగొనవచ్చు. మాకు మరింత ఆచరణాత్మక పద్ధతి ఉంది, ఇది రసాయన మూలకం యొక్క విభిన్న ఐసోటోపుల గురించి సమాచారం మీద ఆధారపడి ఉంటుంది.
దశలు
2 యొక్క 1 వ భాగం: సగటు ద్రవ్యరాశి అణువును లెక్కించండి
ఐసోటోపులు మరియు ద్రవ్యరాశి అణువులను అర్థం చేసుకోండి. ప్రకృతిలో, చాలా అంశాలు అనేక రూపాల్లో లేదా ఐసోటోపులలో ఉన్నాయి. ఒకే మూలకం యొక్క రెండు ఐసోటోపుల మధ్య ఉన్న తేడా ఏమిటంటే అణువులోని న్యూట్రాన్ల సంఖ్య, దీని న్యూట్రాన్ల సంఖ్య ద్రవ్యరాశి అణువును ప్రభావితం చేస్తుంది. సగటు ద్రవ్యరాశి అణువును లెక్కించడం ఈ వ్యత్యాసం యొక్క ప్రభావాన్ని పరిగణనలోకి తీసుకుంటుంది మరియు ఆ అణువుల నమూనాలో ప్రతి అణువు యొక్క సగటు ద్రవ్యరాశిని మీకు చెబుతుంది.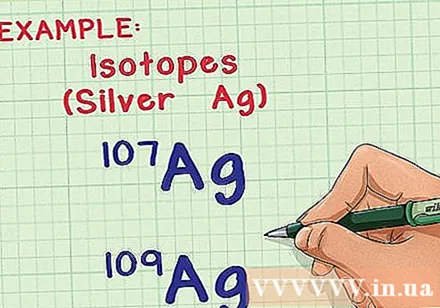
- ఉదాహరణకు, మూలకం వెండి (Ag) రెండు సహజ ఐసోటోపులను కలిగి ఉంది: Ag-107 మరియు Ag-109 (లేదా Ag మరియు Ag). ఐసోటోప్కు "ద్రవ్యరాశి సంఖ్య" లేదా ప్రోటాన్ల సంఖ్య మరియు అణువులోని న్యూట్రాన్ల సంఖ్య పేరు పెట్టబడింది. దీని అర్థం Ag-109 కంటే Ag-107 కంటే రెండు న్యూట్రాన్లు ఉన్నాయి, కాబట్టి దాని అణువు కొంచెం బరువుగా ఉంటుంది.
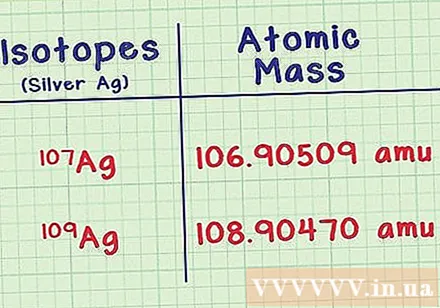
ప్రతి ఐసోటోప్ యొక్క ద్రవ్యరాశిని కనుగొనండి. ప్రతి ఐసోటోప్ కోసం మీకు రెండు సమాచారం అవసరం, మీరు వాటిని రిఫరెన్స్ పుస్తకాలలో చూడవచ్చు లేదా ఆన్లైన్లో చూడవచ్చు, ఉదాహరణకు webelements.com. మొదటిది ప్రతి ఐసోటోప్ యొక్క ద్రవ్యరాశి అణువు లేదా పరమాణు ద్రవ్యరాశి. ఎక్కువ న్యూట్రాన్లు కలిగిన ఐసోటోపులు ఎక్కువ ద్రవ్యరాశిని కలిగి ఉంటాయి.- ఉదాహరణకు, వెండి ఐసోటోప్ Ag-107 ద్రవ్యరాశి అణువును కలిగి ఉంది 106,90509 అము (క్యూబిక్ అణువు యొక్క యూనిట్). ఐసోటోప్ ఎగ్ -109 ద్రవ్యరాశితో కొంచెం బరువుగా ఉంటుంది 108,90470.
- చివర దశాంశాల జత పత్రాలలో కొద్దిగా భిన్నంగా ఉంటుంది. ద్రవ్యరాశి తరువాత కుండలీకరణాల్లో సంఖ్యలను వ్రాయవద్దు.

ప్రతి ఐసోటోప్ కోసం సహజ మనుగడ రేటును వ్రాయండి. ఈ నిష్పత్తి మూలకం యొక్క మొత్తం అణువులలో ఒక శాతంగా ఐసోటోప్ యొక్క ప్రాబల్యాన్ని సూచిస్తుంది. మీరు ఈ సమాచారాన్ని అదే పత్రంలో క్యూబిక్ అణువుతో కనుగొనవచ్చు. అన్ని ఐసోటోపుల యొక్క సహజ మనుగడ 100% ఉండాలి (ఇది రౌండింగ్ లోపం కారణంగా కొద్దిగా తేడా ఉండవచ్చు).- Ag-107 ఐసోటోప్ 51.86% నిష్పత్తిని కలిగి ఉంది. ఐసోటోప్ Ag-109 48.14% చొప్పున తక్కువ సాధారణం. అంటే సాధారణ వెండి నమూనాలో 51.86% Ag-107 మరియు 48.14% Ag-109 ఉన్నాయి.
- ఈ మనుగడ రేటు లేని ఏదైనా ఐసోటోపులు విస్మరించబడతాయి. ఈ ఐసోటోపులు భూమిపై సహజంగా ఉండవు.

ఐసోటోప్ శాతాన్ని దశాంశ సంఖ్యకు మార్చండి. ఈ నిష్పత్తిని 100 ద్వారా భాగించడం దశాంశానికి సమానమైన విలువను ఇస్తుంది.- పై వెండి నమూనాలో, ఐసోటోపుల నిష్పత్తి 51.86 / 100 = 0,5186 మరియు 48,14 / 100 = 0,4814.
సగటు క్యూబిక్ అణువును కనుగొనండి. ఒక మూలకం యొక్క సగటు ద్రవ్యరాశి అణువు ఉంటుంది n ఐసోటోపులు సమానం (అటామిక్ బ్లాక్ఐసోటోప్ 1 * నిష్పత్తిఐసోటోప్ 1) + (పరమాణు ద్రవ్యరాశిఐసోటోప్ 2 * నిష్పత్తిఐసోటోప్ 2) + ... + (పరమాణు ద్రవ్యరాశిఐసోటోపులు n * నిష్పత్తిఐసోటోపులు n. ఇది "సగటు ద్రవ్యరాశి" కి ఉదాహరణ, అనగా ఐసోటోప్ యొక్క మనుగడ రేటు ఎక్కువ, ఫలితంపై దాని ప్రభావం ఎక్కువ. వెండి కోసం ఈ సూత్రాన్ని ఎలా ఉపయోగించాలో ఈ క్రింది విధంగా ఉంది:
- మధ్యస్థ ద్రవ్యరాశి అణువుఎగ్ = (క్యూబిక్ అణువుAg-107 * నిష్పత్తిAg-107) + (పరమాణు ద్రవ్యరాశిఎగ్ -109 * నిష్పత్తిఎగ్ -109)
=(106,90509 * 0,5186) + (108,90470 * 0,4814)
= 55,4410 + 52,4267
= 107.8677 అము. - ఫలితాలను తనిఖీ చేయడానికి ఆ మూలకాన్ని ఆవర్తన పట్టికలో కనుగొనండి. సగటు క్యూబిక్ అణువు ఎల్లప్పుడూ మూలకం యొక్క రసాయన చిహ్నం క్రింద వ్రాయబడుతుంది.
- మధ్యస్థ ద్రవ్యరాశి అణువుఎగ్ = (క్యూబిక్ అణువుAg-107 * నిష్పత్తిAg-107) + (పరమాణు ద్రవ్యరాశిఎగ్ -109 * నిష్పత్తిఎగ్ -109)
2 యొక్క 2 వ భాగం: ఫలితాలను ఉపయోగించడం
ద్రవ్యరాశిని అణు సంఖ్యకు మార్చండి. సగటు క్యూబిక్ అణువు ఆ మూలకం యొక్క సాధారణ నమూనాలో ద్రవ్యరాశి మరియు అణువుల సంఖ్య మధ్య సంబంధాన్ని చూపుతుంది. రసాయన ప్రయోగశాలలలో ఇది చాలా ఉపయోగకరంగా ఉంటుంది ఎందుకంటే అణువులను ఖచ్చితంగా లెక్కించడం దాదాపు అసాధ్యం, కాని ద్రవ్యరాశిని గుర్తించడం సులభం. ఉదాహరణకు, మీరు వెండి నమూనా బరువు మరియు ప్రతి 107,8677 అములకు ఒక వెండి అణువు ఉంటుందని తెలుసుకోవచ్చు.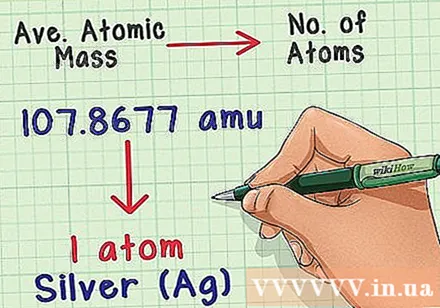
మోలార్ ద్రవ్యరాశిగా మార్చండి. అణు ద్రవ్యరాశి యూనిట్ చాలా చిన్నది, కాబట్టి రసాయన శాస్త్రవేత్తలు తరచూ గ్రామ్ యూనిట్ను ద్రవ్యరాశి కోసం ఉపయోగిస్తారు. అదృష్టవశాత్తూ మనకు ఈ భావనలకు నిర్వచనాలు ఉన్నాయి కాబట్టి పరివర్తన సులభంగా ఉండాలి. G / mol లో ఫలితాన్ని పొందడానికి సగటు ద్రవ్యరాశి అణువును 1 g / mol (మోలార్ మాస్ స్థిరాంకం) ద్వారా గుణించండి. ఉదాహరణకు, 107,8677 గ్రాముల వెండి ఒక మోల్ వెండి అణువులను కలిగి ఉంటుంది.
సగటు పరమాణు ద్రవ్యరాశిని కనుగొనండి. అణువు అణువుల సమాహారం కాబట్టి, పరమాణు ద్రవ్యరాశిని కనుగొనడానికి మీరు అన్ని అణువుల ద్రవ్యరాశిని జోడించవచ్చు. మీరు సగటు ద్రవ్యరాశి అణువును ఉపయోగించినట్లయితే (ఒక నిర్దిష్ట ఐసోటోప్ యొక్క ద్రవ్యరాశికి బదులుగా), ఫలితం ప్రకృతిలో ఒక నమూనా యొక్క సగటు పరమాణు ద్రవ్యరాశి అవుతుంది. ఇక్కడ ఒక ఉదాహరణ: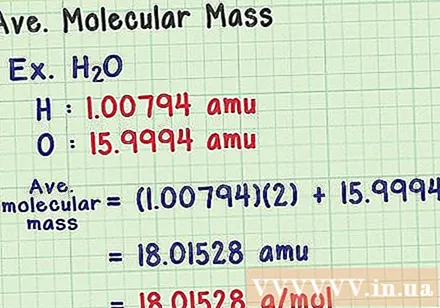
- నీటి అణువులో H అనే రసాయన సూత్రం ఉంది2O లో రెండు హైడ్రోజన్ అణువులు (H) మరియు ఒక ఆక్సిజన్ (O) అణువు ఉంటాయి.
- హైడ్రోజన్ సగటు ద్రవ్యరాశి అణువు 1,00794 అము. ఆక్సిజన్ సగటు అణు ద్రవ్యరాశి 15,9994 అము.
- కాబట్టి H యొక్క సగటు పరమాణు ద్రవ్యరాశి2O (1,00794) (2) + 15,9994 = 18,01528 అము, ఇది 18,01528 గ్రా / మోల్కు సమానం.
సలహా
- సాపేక్ష అణు ద్రవ్యరాశి యొక్క భావన కొన్నిసార్లు మధ్యస్థ ద్రవ్యరాశి అణువుతో పర్యాయపదంగా ఉపయోగించబడుతుంది. స్వల్ప వ్యత్యాసం ఉంది ఎందుకంటే పరమాణు ద్రవ్యరాశి సాపేక్షంగా అన్ యూనిట్; ఇది కార్బన్ -12 అణువుకు సంబంధించి ద్రవ్యరాశి యొక్క కొలత. మీరు సగటు క్యూబిక్ అణువు గణనలో అణు ద్రవ్యరాశి యూనిట్ను ఉపయోగిస్తున్నంత కాలం, ఈ రెండు విలువలు ఒకే విధంగా ఉంటాయి.
- క్యూబిక్ అణువు తర్వాత కుండలీకరణాల్లోని సంఖ్య మనకు లోపం చెబుతుంది. ఉదాహరణకు, ద్రవ్యరాశి అణువు 1.0173 (4) అంటే మూలకం యొక్క సాధారణ అణువు సుమారు 1.0173 ± 0.0004 ద్రవ్యరాశి పరిధిని కలిగి ఉంటుంది. అభ్యర్థించకపోతే మీరు ఈ సంఖ్యను పొందవలసిన అవసరం లేదు.
- ఆవర్తన పట్టికలో, కింది మూలకం యొక్క సగటు క్యూబిక్ అణువు దాని ముందు ఉన్నదానికంటే పెద్దది, కొన్ని మినహాయింపులతో. మీ ఫలితాలను తనిఖీ చేయడానికి శీఘ్ర మార్గం ఇక్కడ ఉంది.
- 1 పరమాణు ద్రవ్యరాశి యూనిట్ కార్బన్ -12 అణువు యొక్క ద్రవ్యరాశి 1/12.
- ఐసోటోప్ మనుగడ రేట్లు భూమిపై సహజంగా సంభవించే నమూనాల ప్రకారం లెక్కించబడతాయి. సహజంగా సంభవించే ఉల్కలు లేదా ప్రయోగశాలలో ఉత్పత్తి చేయబడిన పదార్థాలు వేర్వేరు ఐసోటోప్ నిష్పత్తులను కలిగి ఉంటాయి, కాబట్టి సగటు ద్రవ్యరాశి అణువు కూడా భిన్నంగా ఉంటుంది.
హెచ్చరిక
- ద్రవ్యరాశి అణువులను ఎల్లప్పుడూ అణు ద్రవ్యరాశి యూనిట్లలో (అము లేదా యు) వ్రాస్తారు, దీనిని కొన్నిసార్లు డాల్టన్స్ (డా) అని పిలుస్తారు. ఈ సంఖ్యను మార్చకుండా మరొక యూనిట్ ద్రవ్యరాశిని (కిలోగ్రాము వంటివి) ఎప్పుడూ వ్రాయవద్దు.
నీకు కావాల్సింది ఏంటి
- పెన్సిల్
- పేపర్
- ల్యాప్టాప్
- ప్రకృతిలో ఐసోటోప్ మనుగడ రేటుపై డేటా.
- ఐసోటోపుల కోసం మాస్ అణు యూనిట్ డేటా.