రచయిత:
Christy White
సృష్టి తేదీ:
8 మే 2021
నవీకరణ తేదీ:
1 జూలై 2024

విషయము
- అడుగు పెట్టడానికి
- 3 యొక్క విధానం 1: మొదటి భాగం: ఎలక్ట్రాన్ షెల్స్ను అర్థం చేసుకోవడం
- 3 యొక్క విధానం 2: రెండవ భాగం: పరివర్తన లోహాలు తప్ప, లోహాలలో వాలెన్స్ ఎలక్ట్రాన్లను కనుగొనడం
- 3 యొక్క విధానం 3: మూడవ భాగం: పరివర్తన లోహాలలో వాలెన్స్ ఎలక్ట్రాన్లను కనుగొనడం
- చిట్కాలు
- అవసరాలు
వాలెన్స్ ఎలక్ట్రాన్లు ఒక మూలకం యొక్క బయటి షెల్లో ఉంటాయి. అణువులోని వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్య ఈ మూలకం ఏర్పడే రసాయన బంధం యొక్క రకాన్ని నిర్ణయిస్తుంది. మూలకాల యొక్క ఆవర్తన పట్టికను ఉపయోగించడం వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యను తెలుసుకోవడానికి ఉత్తమ మార్గం.
అడుగు పెట్టడానికి
3 యొక్క విధానం 1: మొదటి భాగం: ఎలక్ట్రాన్ షెల్స్ను అర్థం చేసుకోవడం
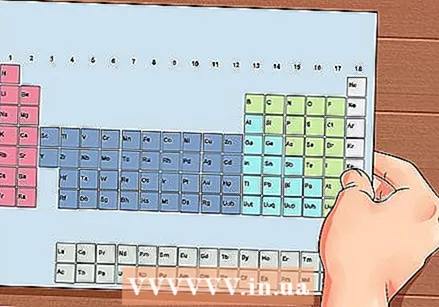 మూలకాల యొక్క ఆవర్తన పట్టిక. ఇది రంగు సంకేతాలతో కూడిన పట్టిక, ఇక్కడ ప్రతి కణంలో ఒక మూలకం పరమాణు సంఖ్యతో మరియు 1 నుండి 3 అక్షరాలతో చిహ్నంగా ప్రదర్శించబడుతుంది.
మూలకాల యొక్క ఆవర్తన పట్టిక. ఇది రంగు సంకేతాలతో కూడిన పట్టిక, ఇక్కడ ప్రతి కణంలో ఒక మూలకం పరమాణు సంఖ్యతో మరియు 1 నుండి 3 అక్షరాలతో చిహ్నంగా ప్రదర్శించబడుతుంది. 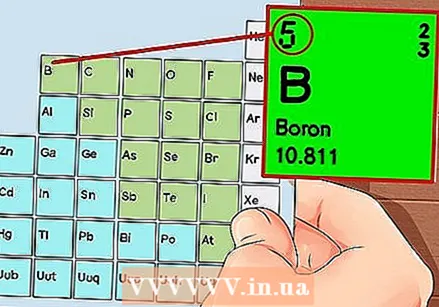 మూలకం యొక్క పరమాణు సంఖ్యను కనుగొనండి. పరమాణు సంఖ్య మూలకం యొక్క చిహ్నం పైన లేదా పక్కన ఉంది. ఉదాహరణకు: బోరాన్ (బి) 5 యొక్క పరమాణు సంఖ్యను కలిగి ఉంది, అంటే దీనికి 5 ప్రోటాన్లు మరియు 5 ఎలక్ట్రాన్లు ఉన్నాయి.
మూలకం యొక్క పరమాణు సంఖ్యను కనుగొనండి. పరమాణు సంఖ్య మూలకం యొక్క చిహ్నం పైన లేదా పక్కన ఉంది. ఉదాహరణకు: బోరాన్ (బి) 5 యొక్క పరమాణు సంఖ్యను కలిగి ఉంది, అంటే దీనికి 5 ప్రోటాన్లు మరియు 5 ఎలక్ట్రాన్లు ఉన్నాయి. 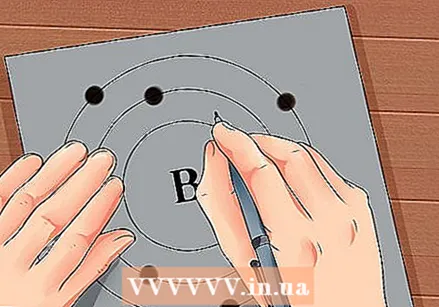 అణువు యొక్క సరళమైన ప్రాతినిధ్యాన్ని గీయండి మరియు ఎలక్ట్రాన్లను కేంద్రకం చుట్టూ కక్ష్యలో ఉంచండి. ఈ ఉద్యోగాలను షెల్స్ లేదా ఎనర్జీ లెవల్స్ అని కూడా అంటారు. ఒకే షెల్లో ఉండే ఎలక్ట్రాన్ల గరిష్ట సంఖ్య పరిష్కరించబడింది మరియు షెల్స్ లోపలి నుండి బయటి కక్ష్య వరకు నిండి ఉంటాయి.
అణువు యొక్క సరళమైన ప్రాతినిధ్యాన్ని గీయండి మరియు ఎలక్ట్రాన్లను కేంద్రకం చుట్టూ కక్ష్యలో ఉంచండి. ఈ ఉద్యోగాలను షెల్స్ లేదా ఎనర్జీ లెవల్స్ అని కూడా అంటారు. ఒకే షెల్లో ఉండే ఎలక్ట్రాన్ల గరిష్ట సంఖ్య పరిష్కరించబడింది మరియు షెల్స్ లోపలి నుండి బయటి కక్ష్య వరకు నిండి ఉంటాయి. - కె షెల్ (లోపలి): గరిష్టంగా 2 ఎలక్ట్రాన్లు.
- ఎల్ షెల్: గరిష్టంగా 8 ఎలక్ట్రాన్లు.
- M షెల్: గరిష్టంగా 18 ఎలక్ట్రాన్లు.
- ఎన్ షెల్: గరిష్టంగా 32 ఎలక్ట్రాన్లు.
- ఓ షెల్: గరిష్టంగా 50 ఎలక్ట్రాన్లు.
- పి షెల్ (బయటి): గరిష్టంగా 72 ఎలక్ట్రాన్లు.
 బయటి షెల్లో ఎలక్ట్రాన్ల సంఖ్యను కనుగొనండి. ఇవి వాలెన్స్ ఎలక్ట్రాన్లు.
బయటి షెల్లో ఎలక్ట్రాన్ల సంఖ్యను కనుగొనండి. ఇవి వాలెన్స్ ఎలక్ట్రాన్లు. - వాలెన్స్ షెల్ నిండినప్పుడు, మూలకం స్థిరంగా ఉంటుంది.
- వాలెన్స్ షెల్ పూర్తి కాకపోతే మూలకం రియాక్టివ్గా ఉంటుంది, అంటే ఇది మరొక మూలకం యొక్క అణువుతో రసాయనికంగా బంధించగలదు. ప్రతి అణువు వాలెన్స్ షెల్ ని పూర్తి చేసే ప్రయత్నంలో దాని వాలెన్స్ ఎలక్ట్రాన్లను పంచుకుంటుంది.
3 యొక్క విధానం 2: రెండవ భాగం: పరివర్తన లోహాలు తప్ప, లోహాలలో వాలెన్స్ ఎలక్ట్రాన్లను కనుగొనడం
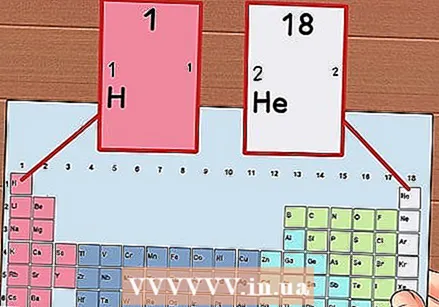 ఆవర్తన పట్టికలోని ప్రతి కాలమ్ను 1 నుండి 18 వరకు సంఖ్య చేయండి. హైడ్రోజన్ (హెచ్) కాలమ్ 1 పైభాగంలో మరియు హీలియం (హి) కాలమ్ 18 పైభాగంలో ఉంటుంది. ఇవి మూలకాల యొక్క విభిన్న సమూహాలు.
ఆవర్తన పట్టికలోని ప్రతి కాలమ్ను 1 నుండి 18 వరకు సంఖ్య చేయండి. హైడ్రోజన్ (హెచ్) కాలమ్ 1 పైభాగంలో మరియు హీలియం (హి) కాలమ్ 18 పైభాగంలో ఉంటుంది. ఇవి మూలకాల యొక్క విభిన్న సమూహాలు. 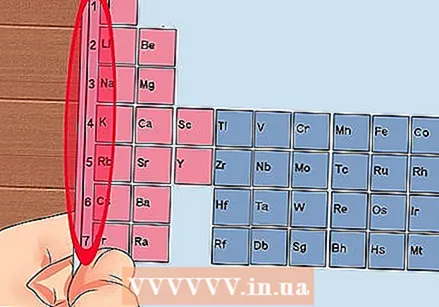 ప్రతి అడ్డు వరుసకు 1 నుండి 7 వరకు సంఖ్య ఇవ్వండి. ఇవి మూలకాల కాలాలు, మరియు అవి అణువు యొక్క గుండ్లు లేదా శక్తి స్థాయిలకు అనుగుణంగా ఉంటాయి.
ప్రతి అడ్డు వరుసకు 1 నుండి 7 వరకు సంఖ్య ఇవ్వండి. ఇవి మూలకాల కాలాలు, మరియు అవి అణువు యొక్క గుండ్లు లేదా శక్తి స్థాయిలకు అనుగుణంగా ఉంటాయి. - హైడ్రోజన్ (H) మరియు హీలియం (అతను) రెండూ 1 షెల్ కలిగి ఉండగా, ఫ్రాన్షియం (Fr) 7 కలిగి ఉంది.
- లాంతనైడ్లు మరియు ఆక్టినైడ్లు సమూహం చేయబడ్డాయి మరియు ప్రధాన పట్టిక క్రింద ఇవ్వబడ్డాయి. అన్ని లాంతనైడ్లు పీరియడ్ 6, గ్రూప్ 3 కి చెందినవి మరియు అన్ని యాక్టినైడ్లు పీరియడ్ 7, గ్రూప్ 3 కి చెందినవి.
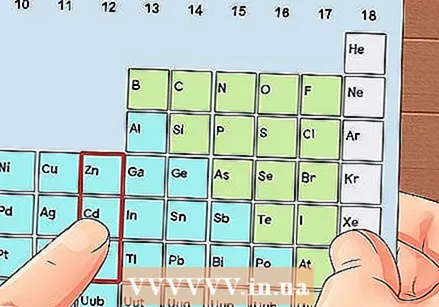 పరివర్తన లోహం లేని మూలకాన్ని గుర్తించండి. పరివర్తన లోహాలు 3 నుండి 12 సమూహాలలో ఉంటాయి. ఇతర లోహాల సమూహ సంఖ్యలు వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యను సూచిస్తాయి.
పరివర్తన లోహం లేని మూలకాన్ని గుర్తించండి. పరివర్తన లోహాలు 3 నుండి 12 సమూహాలలో ఉంటాయి. ఇతర లోహాల సమూహ సంఖ్యలు వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యను సూచిస్తాయి. - సమూహం 1: 1 వాలెన్స్ ఎలక్ట్రాన్
- సమూహం 2: 2 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 13: 3 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 14: 4 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 15: 5 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 16: 6 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 17: 7 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 18: 8 వాలెన్స్ ఎలక్ట్రాన్లు - హీలియం తప్ప, ఇందులో 2 ఉన్నాయి
3 యొక్క విధానం 3: మూడవ భాగం: పరివర్తన లోహాలలో వాలెన్స్ ఎలక్ట్రాన్లను కనుగొనడం
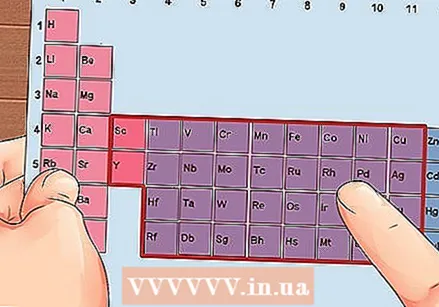 సమూహాల 3 నుండి 12 వరకు పరివర్తన లోహాలను కనుగొనండి.
సమూహాల 3 నుండి 12 వరకు పరివర్తన లోహాలను కనుగొనండి. సమూహ సంఖ్య ఆధారంగా వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యను నిర్ణయించండి. ఈ సమూహ సంఖ్యలు సాధ్యమైన సంఖ్యలో వాలెన్స్ ఎలక్ట్రాన్లకు అనుగుణంగా ఉంటాయి.
సమూహ సంఖ్య ఆధారంగా వాలెన్స్ ఎలక్ట్రాన్ల సంఖ్యను నిర్ణయించండి. ఈ సమూహ సంఖ్యలు సాధ్యమైన సంఖ్యలో వాలెన్స్ ఎలక్ట్రాన్లకు అనుగుణంగా ఉంటాయి. - సమూహం 3: 3 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 4: 2 నుండి 4 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 5: 2 నుండి 5 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 6: 2 నుండి 6 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 7: 2 నుండి 7 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 8: 2 లేదా 3 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 9: 2 లేదా 3 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 10: 2 లేదా 3 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 11: 1 లేదా 2 వాలెన్స్ ఎలక్ట్రాన్లు
- సమూహం 12: 2 వాలెన్స్ ఎలక్ట్రాన్లు
చిట్కాలు
- పరివర్తన లోహాలు పూర్తిగా నిండిన వాలెన్స్ షెల్స్ను కలిగి ఉంటాయి. పరివర్తన లోహాలలో వాలెన్స్ ఎలక్ట్రాన్ల యొక్క ఖచ్చితమైన సంఖ్యను నిర్ణయించడానికి ఈ కాగితం పరిధికి మించిన క్వాంటం సిద్ధాంతం యొక్క కొన్ని సూత్రాలు అవసరం.
అవసరాలు
- మూలకాల యొక్క ఆవర్తన పట్టిక
- పెన్సిల్
- పేపర్