రచయిత:
Eugene Taylor
సృష్టి తేదీ:
12 ఆగస్టు 2021
నవీకరణ తేదీ:
22 జూన్ 2024

విషయము
- అడుగు పెట్టడానికి
- 2 యొక్క పార్ట్ 1: ఒక మూలకం యొక్క సాధారణ ఎలక్ట్రాన్ కాన్ఫిగరేషన్
- 2 యొక్క 2 వ భాగం: నోబెల్ గ్యాస్ ఎలక్ట్రాన్ కాన్ఫిగరేషన్
- హెచ్చరికలు
ఒక మూలకం కోసం ఎలక్ట్రాన్ కాన్ఫిగరేషన్ రాయడం అణువులోని ఎలక్ట్రాన్ల పంపిణీని చూడటానికి మంచి మార్గం. మూలకాన్ని బట్టి, సూత్రం చాలా పొడవుగా ఉంటుంది. అందువల్ల, శాస్త్రవేత్తలు సంక్షిప్తలిపి సంజ్ఞామానాన్ని అభివృద్ధి చేశారు, ఇది వాలెన్స్ ఎలక్ట్రాన్లు కాని ఎలక్ట్రాన్లను సూచించడానికి ఒక గొప్ప వాయువును ఉపయోగిస్తుంది. ఇది ఎలక్ట్రాన్ కాన్ఫిగరేషన్ను సులభతరం చేస్తుంది మరియు మూలకం యొక్క రసాయన లక్షణాలను అర్థం చేసుకోవడం సులభం చేస్తుంది.
అడుగు పెట్టడానికి
2 యొక్క పార్ట్ 1: ఒక మూలకం యొక్క సాధారణ ఎలక్ట్రాన్ కాన్ఫిగరేషన్
 మూలకంలో ఉన్న ఎలక్ట్రాన్ల సంఖ్యను నిర్ణయించండి. ఒక మూలకం యొక్క పరమాణు సంఖ్య దానిలోని ప్రోటాన్ల సంఖ్యను మీకు చెబుతుంది. వాటి తటస్థ స్థితిలో ఉన్న మూలకాలు ఒకే సంఖ్యలో ప్రోటాన్లు మరియు ఎలక్ట్రాన్లను కలిగి ఉన్నందున, మూలకం ఉన్న ఎలక్ట్రాన్ల సంఖ్య వలె మీరు పరమాణు సంఖ్యను కూడా ఉపయోగించవచ్చు. ఆవర్తన పట్టికలో మీరు కనుగొనగల పరమాణు సంఖ్య, మూలకం యొక్క గుర్తుకు నేరుగా పైన ఉన్న సంఖ్య.
మూలకంలో ఉన్న ఎలక్ట్రాన్ల సంఖ్యను నిర్ణయించండి. ఒక మూలకం యొక్క పరమాణు సంఖ్య దానిలోని ప్రోటాన్ల సంఖ్యను మీకు చెబుతుంది. వాటి తటస్థ స్థితిలో ఉన్న మూలకాలు ఒకే సంఖ్యలో ప్రోటాన్లు మరియు ఎలక్ట్రాన్లను కలిగి ఉన్నందున, మూలకం ఉన్న ఎలక్ట్రాన్ల సంఖ్య వలె మీరు పరమాణు సంఖ్యను కూడా ఉపయోగించవచ్చు. ఆవర్తన పట్టికలో మీరు కనుగొనగల పరమాణు సంఖ్య, మూలకం యొక్క గుర్తుకు నేరుగా పైన ఉన్న సంఖ్య. - ఉదాహరణకు, సోడియం యొక్క చిహ్నం Na. Na యొక్క పరమాణు సంఖ్య 11.
 ఎలక్ట్రాన్ గుండ్లు మరియు శక్తి స్థాయిల గురించి జ్ఞానం. మొదటి ఎలక్ట్రాన్ షెల్ s శక్తి స్థాయిని మాత్రమే కలిగి ఉంటుంది, రెండవ ఎలక్ట్రాన్ షెల్ s మరియు p శక్తి స్థాయి రెండింటినీ కలిగి ఉంటుంది. మూడవ ఎలక్ట్రాన్ షెల్ s, p మరియు d శక్తి స్థాయిని కలిగి ఉంటుంది. నాల్గవ ఎలక్ట్రాన్ షెల్ s, p, d మరియు f శక్తి స్థాయిని కలిగి ఉంటుంది. నాలుగు కంటే ఎక్కువ ఎలక్ట్రాన్ గుండ్లు ఉన్నాయి, కానీ హైస్కూల్ కెమిస్ట్రీలో మీరు సాధారణంగా మొదటి నాలుగు మాత్రమే ఎదుర్కొంటారు.
ఎలక్ట్రాన్ గుండ్లు మరియు శక్తి స్థాయిల గురించి జ్ఞానం. మొదటి ఎలక్ట్రాన్ షెల్ s శక్తి స్థాయిని మాత్రమే కలిగి ఉంటుంది, రెండవ ఎలక్ట్రాన్ షెల్ s మరియు p శక్తి స్థాయి రెండింటినీ కలిగి ఉంటుంది. మూడవ ఎలక్ట్రాన్ షెల్ s, p మరియు d శక్తి స్థాయిని కలిగి ఉంటుంది. నాల్గవ ఎలక్ట్రాన్ షెల్ s, p, d మరియు f శక్తి స్థాయిని కలిగి ఉంటుంది. నాలుగు కంటే ఎక్కువ ఎలక్ట్రాన్ గుండ్లు ఉన్నాయి, కానీ హైస్కూల్ కెమిస్ట్రీలో మీరు సాధారణంగా మొదటి నాలుగు మాత్రమే ఎదుర్కొంటారు. - ప్రతి శక్తి స్థాయి 2 ఎలక్ట్రాన్ల వరకు ఉంటుంది.
- ప్రతి p శక్తి స్థాయి 6 ఎలక్ట్రాన్ల వరకు ఉంటుంది.
- ప్రతి d శక్తి స్థాయి 10 ఎలక్ట్రాన్లను కలిగి ఉంటుంది.
- ప్రతి f శక్తి స్థాయి 14 ఎలక్ట్రాన్ల వరకు ఉంటుంది.
 ఎలక్ట్రాన్ నింపే నియమాలను తెలుసుకోండి. Uf ఫ్బా సూత్రం ప్రకారం, ఎలక్ట్రాన్ను అధిక శక్తి స్థాయికి చేర్చడానికి ముందు మీరు ఎలక్ట్రాన్లను అత్యల్ప శక్తి స్థాయిలకు చేర్చాలి. ప్రతి శక్తి స్థాయికి బహుళ సబార్బిటల్స్ ఉండవచ్చు, కానీ ప్రతి సబోర్బిటల్ ఏ సమయంలోనైనా రెండు ఎలక్ట్రాన్ల వరకు పట్టుకోగలదు. S శక్తి స్థాయికి ఒక సబోర్బిటల్ ఉంది, p కి 3 సబార్బిటల్స్ ఉన్నాయి, d కి 5 సబార్బిటల్స్ ఉన్నాయి, మరియు ఎఫ్ 7 సబార్బిటల్స్ కలిగి ఉంది.
ఎలక్ట్రాన్ నింపే నియమాలను తెలుసుకోండి. Uf ఫ్బా సూత్రం ప్రకారం, ఎలక్ట్రాన్ను అధిక శక్తి స్థాయికి చేర్చడానికి ముందు మీరు ఎలక్ట్రాన్లను అత్యల్ప శక్తి స్థాయిలకు చేర్చాలి. ప్రతి శక్తి స్థాయికి బహుళ సబార్బిటల్స్ ఉండవచ్చు, కానీ ప్రతి సబోర్బిటల్ ఏ సమయంలోనైనా రెండు ఎలక్ట్రాన్ల వరకు పట్టుకోగలదు. S శక్తి స్థాయికి ఒక సబోర్బిటల్ ఉంది, p కి 3 సబార్బిటల్స్ ఉన్నాయి, d కి 5 సబార్బిటల్స్ ఉన్నాయి, మరియు ఎఫ్ 7 సబార్బిటల్స్ కలిగి ఉంది. - D శక్తి స్థాయి తక్కువ ఎలక్ట్రాన్ షెల్ యొక్క శక్తి స్థాయి కంటే కొంచెం ఎక్కువ శక్తిని కలిగి ఉంటుంది, కాబట్టి అధిక శక్తి స్థాయి తక్కువ d శక్తి స్థాయి కంటే నింపే అవకాశం ఉంది. ఎలక్ట్రాన్ కాన్ఫిగరేషన్ రాయడానికి, ఇది ఇలా కనిపిస్తుంది: 1s2s2p3s3p4s3d.
 ఎలక్ట్రాన్ కాన్ఫిగరేషన్లను వ్రాయడానికి వికర్ణ కాన్ఫిగరేషన్ గ్రాఫ్ ఉపయోగించండి. ఎలక్ట్రాన్లు ఎలా నింపుతాయో గుర్తుంచుకోవడానికి సులభమైన మార్గం కాన్ఫిగరేషన్ స్కీమ్ను ఉపయోగించడం. దీనిలో మీరు ప్రతి షెల్ మరియు శక్తి స్థాయిలను వ్రాస్తారు. ప్రతి పంక్తికి ఎగువ కుడి నుండి దిగువ ఎడమవైపు వికర్ణ రేఖలను గీయండి. కాన్ఫిగరేషన్ పథకం క్రింది విధంగా ఉంది:
ఎలక్ట్రాన్ కాన్ఫిగరేషన్లను వ్రాయడానికి వికర్ణ కాన్ఫిగరేషన్ గ్రాఫ్ ఉపయోగించండి. ఎలక్ట్రాన్లు ఎలా నింపుతాయో గుర్తుంచుకోవడానికి సులభమైన మార్గం కాన్ఫిగరేషన్ స్కీమ్ను ఉపయోగించడం. దీనిలో మీరు ప్రతి షెల్ మరియు శక్తి స్థాయిలను వ్రాస్తారు. ప్రతి పంక్తికి ఎగువ కుడి నుండి దిగువ ఎడమవైపు వికర్ణ రేఖలను గీయండి. కాన్ఫిగరేషన్ పథకం క్రింది విధంగా ఉంది: - 1 సె
2 సె 2 పి
3 సె 3 పి 3 డి
4s 4p 4d 4f
5s 5p 5d 5f
6 సె 6 పి 6 డి
7 సె 7 పి - ఉదాహరణకు: సోడియం (11 ఎలక్ట్రాన్లు) యొక్క ఎలక్ట్రాన్ కాన్ఫిగరేషన్: 1s2s2p3s.
- 1 సె
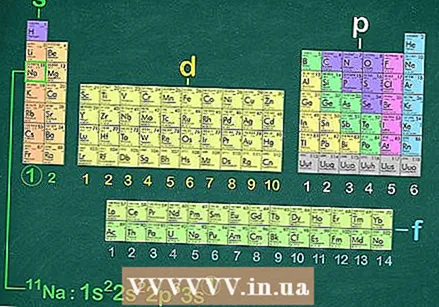 ప్రతి కాన్ఫిగరేషన్ యొక్క చివరి కక్ష్యను నిర్ణయించండి. ఆవర్తన పట్టికను చూడటం ద్వారా, ఎలక్ట్రాన్ కాన్ఫిగరేషన్ యొక్క చివరి సబ్షెల్ మరియు చివరి శక్తి స్థాయి ఏమిటో మీరు నిర్ణయించవచ్చు. మూలకం ఏ బ్లాక్లో పడుతుందో ముందుగా నిర్ణయించండి (లు, పి, డి లేదా ఎఫ్). మూలకం ఏ వరుసలో ఉందో లెక్కించండి. చివరగా, మూలకం ఏ కాలమ్లో ఉందో లెక్కించండి.
ప్రతి కాన్ఫిగరేషన్ యొక్క చివరి కక్ష్యను నిర్ణయించండి. ఆవర్తన పట్టికను చూడటం ద్వారా, ఎలక్ట్రాన్ కాన్ఫిగరేషన్ యొక్క చివరి సబ్షెల్ మరియు చివరి శక్తి స్థాయి ఏమిటో మీరు నిర్ణయించవచ్చు. మూలకం ఏ బ్లాక్లో పడుతుందో ముందుగా నిర్ణయించండి (లు, పి, డి లేదా ఎఫ్). మూలకం ఏ వరుసలో ఉందో లెక్కించండి. చివరగా, మూలకం ఏ కాలమ్లో ఉందో లెక్కించండి. - ఉదాహరణకు, సోడియం s బ్లాక్లో ఉంది, కాబట్టి దాని ఎలక్ట్రాన్ కాన్ఫిగరేషన్ యొక్క చివరి కక్ష్య s. ఇది మూడవ వరుసలో మరియు మొదటి కాలమ్లో ఉంది, కాబట్టి చివరి కక్ష్య 3 సె. మీ తుది జవాబును తనిఖీ చేయడానికి ఇది మంచి మార్గం.
- D కక్ష్యకు నియమం కొంచెం భిన్నంగా ఉంటుంది. D- బ్లాక్ మూలకాల యొక్క మొదటి వరుస నాల్గవ వరుసలో మొదలవుతుంది, కాని మీరు అడ్డు వరుస సంఖ్య నుండి 1 ను తీసివేయాలి ఎందుకంటే s స్థాయిలు d స్థాయిల కంటే తక్కువ శక్తిని కలిగి ఉంటాయి. ఉదాహరణకు: వనాడియం 3 డిలో ముగుస్తుంది.
- మీ పనిని తనిఖీ చేయడానికి మరొక మార్గం అన్ని సూపర్స్క్రిప్ట్లను జోడించడం. అవి మూలకంలోని ఎలక్ట్రాన్ల సంఖ్యకు సమానంగా ఉండాలి. మీకు చాలా తక్కువ లేదా ఎక్కువ ఎలక్ట్రాన్లు ఉంటే, మీరు మీ పనిని పునరాలోచించి మళ్ళీ ప్రయత్నించాలి.
2 యొక్క 2 వ భాగం: నోబెల్ గ్యాస్ ఎలక్ట్రాన్ కాన్ఫిగరేషన్
 నోబెల్ గ్యాస్ ఎలక్ట్రాన్ కాన్ఫిగరేషన్ను నిర్ణయించండి. నోబెల్ గ్యాస్ ఎలక్ట్రాన్ కాన్ఫిగరేషన్ అనేది ఒక మూలకం యొక్క పూర్తి ఎలక్ట్రాన్ కాన్ఫిగరేషన్ను వ్రాసే ఒక రకమైన సంక్షిప్తలిపి మార్గం. ఒక మూలకం యొక్క ఎలక్ట్రాన్ ఆకృతీకరణను సంగ్రహించడానికి నోబెల్ గ్యాస్ సంక్షిప్తలిపి ఉపయోగించబడుతుంది, అయితే ఆ మూలకం యొక్క వాలెన్స్ ఎలక్ట్రాన్ల గురించి చాలా సంబంధిత సమాచారాన్ని అందిస్తుంది.
నోబెల్ గ్యాస్ ఎలక్ట్రాన్ కాన్ఫిగరేషన్ను నిర్ణయించండి. నోబెల్ గ్యాస్ ఎలక్ట్రాన్ కాన్ఫిగరేషన్ అనేది ఒక మూలకం యొక్క పూర్తి ఎలక్ట్రాన్ కాన్ఫిగరేషన్ను వ్రాసే ఒక రకమైన సంక్షిప్తలిపి మార్గం. ఒక మూలకం యొక్క ఎలక్ట్రాన్ ఆకృతీకరణను సంగ్రహించడానికి నోబెల్ గ్యాస్ సంక్షిప్తలిపి ఉపయోగించబడుతుంది, అయితే ఆ మూలకం యొక్క వాలెన్స్ ఎలక్ట్రాన్ల గురించి చాలా సంబంధిత సమాచారాన్ని అందిస్తుంది. - వాలెన్స్ ఎలక్ట్రాన్లు కాని అన్ని ఎలక్ట్రాన్లను సూచించడానికి నోబెల్ వాయువు ప్రత్యామ్నాయం.
- గొప్ప వాయువులు హీలియం, నియాన్, ఆర్గాన్, క్రిప్టాన్, జినాన్ మరియు రాడాన్ మరియు ఆవర్తన పట్టిక యొక్క చివరి కాలమ్లో ఉన్నాయి.
 మీ మూలకం కోసం కాలంలో నోబెల్ వాయువును గుర్తించండి. మూలకం యొక్క కాలం మూలకం ఉన్న సమాంతర వరుస. మూలకం ఆవర్తన పట్టిక యొక్క నాల్గవ వరుసలో ఉంటే, అది నాలుగవ వ్యవధిలో ఉంటుంది. మీరు ఉపయోగిస్తున్న నోబెల్ గ్యాస్ మూడవ వ్యవధిలో ఉంది. క్రింద ఉన్న నోబెల్ వాయువుల జాబితా మరియు వాటి కాలాలు:
మీ మూలకం కోసం కాలంలో నోబెల్ వాయువును గుర్తించండి. మూలకం యొక్క కాలం మూలకం ఉన్న సమాంతర వరుస. మూలకం ఆవర్తన పట్టిక యొక్క నాల్గవ వరుసలో ఉంటే, అది నాలుగవ వ్యవధిలో ఉంటుంది. మీరు ఉపయోగిస్తున్న నోబెల్ గ్యాస్ మూడవ వ్యవధిలో ఉంది. క్రింద ఉన్న నోబెల్ వాయువుల జాబితా మరియు వాటి కాలాలు: - 1: హీలియం
- 2: నియాన్
- 3: ఆర్గాన్
- 4: క్రిప్టాన్
- 5: జినాన్
- 6: రాడాన్
- ఉదాహరణకు, సోడియం కాలం 3 లో ఉంది. నోబెల్ గ్యాస్ కాన్ఫిగరేషన్ కోసం మేము నియాన్ను ఉపయోగిస్తాము ఎందుకంటే ఇది కాలం 2 లో ఉంది.
 నోబెల్ వాయువు ఉన్న నోబెల్ వాయువును అదే సంఖ్యలో ఎలక్ట్రాన్లతో భర్తీ చేయండి. ఈ తదుపరి దశ చేయడానికి కొన్ని మార్గాలు ఉన్నాయి. మీరు నోబెల్ వాయువు యొక్క ఎలక్ట్రాన్ కాన్ఫిగరేషన్ను వ్రాసి, ఆపై మీ ఆసక్తి యొక్క మూలకంలో అదే కాన్ఫిగరేషన్ను భర్తీ చేయవచ్చు. ప్రత్యామ్నాయం ఏమిటంటే, మీరు కాన్ఫిగరేషన్ను వ్రాస్తున్న మూలకం నుండి నోబెల్ వాయువు కలిగి ఉన్న అదే సంఖ్యలో ఎలక్ట్రాన్లను తొలగించడం.
నోబెల్ వాయువు ఉన్న నోబెల్ వాయువును అదే సంఖ్యలో ఎలక్ట్రాన్లతో భర్తీ చేయండి. ఈ తదుపరి దశ చేయడానికి కొన్ని మార్గాలు ఉన్నాయి. మీరు నోబెల్ వాయువు యొక్క ఎలక్ట్రాన్ కాన్ఫిగరేషన్ను వ్రాసి, ఆపై మీ ఆసక్తి యొక్క మూలకంలో అదే కాన్ఫిగరేషన్ను భర్తీ చేయవచ్చు. ప్రత్యామ్నాయం ఏమిటంటే, మీరు కాన్ఫిగరేషన్ను వ్రాస్తున్న మూలకం నుండి నోబెల్ వాయువు కలిగి ఉన్న అదే సంఖ్యలో ఎలక్ట్రాన్లను తొలగించడం. - ఉదాహరణకు, సోడియంలో 11 ఎలక్ట్రాన్లు మరియు నియాన్లో 10 ఎలక్ట్రాన్లు ఉన్నాయి.
- సోడియం కోసం పూర్తి ఎలక్ట్రాన్ కాన్ఫిగరేషన్: 1s22p3s మరియు నియాన్ 1s22p. మీరు గమనిస్తే, సోడియంలో నియాన్ లేని 3 సె ఉంది - అందుకే సోడియం కొరకు నోబెల్ గ్యాస్ కాన్ఫిగరేషన్ [Ne] 3 సె అవుతుంది.
- ప్రత్యామ్నాయంగా, మీకు పది వచ్చే వరకు శక్తి స్థాయిల సూపర్స్క్రిప్ట్లను లెక్కించవచ్చు. ఈ శక్తి స్థాయిలను తీసివేసి, మిగిలి ఉన్న వాటిని విడదీయండి. సోడియం కోసం ఎలక్ట్రాన్ కాన్ఫిగరేషన్ను వ్రాయడానికి మీరు నియాన్ను ఉపయోగిస్తే, మీకు ఒక ఎలక్ట్రాన్ మిగిలి ఉంటుంది: [Ne] 3 సె.
హెచ్చరికలు
- తటస్థ అణువులో మాత్రమే పరమాణు సంఖ్య ఎలక్ట్రాన్ల సంఖ్యకు సమానం. ఒక అయాన్ వేరే సంఖ్యలో ఎలక్ట్రాన్లను కలిగి ఉంటుంది. అయాన్ -1 యొక్క ఛార్జ్ కలిగి ఉంటే, దానికి ఒక అదనపు ఎలక్ట్రాన్ ఉంటుంది. ఛార్జ్ -2 లో రెండు అదనపు ఎలక్ట్రాన్లు మొదలైనవి ఉన్నాయి.