రచయిత:
Randy Alexander
సృష్టి తేదీ:
25 ఏప్రిల్ 2021
నవీకరణ తేదీ:
26 జూన్ 2024

విషయము
రసాయన శాస్త్రంలో, కరిగే అవశేషాలను వదలకుండా ద్రవంలో పూర్తిగా కరిగినప్పుడు ఘన సమ్మేళనం యొక్క లక్షణాలను వివరించడానికి కరిగే సామర్థ్యాన్ని ఉపయోగిస్తారు. అయానిక్ సమ్మేళనాలు (చార్జ్ చేయబడినవి) మాత్రమే కరిగేవి. వాస్తవానికి, మీరు నీటిలో కలిపినప్పుడు అయానిక్ సమ్మేళనం దృ solid ంగా ఉంటుందా లేదా పెద్ద మొత్తంలో కరిగిపోతుందో లేదో తెలుసుకోవడానికి మీరు కొన్ని సూత్రాలను మాత్రమే గుర్తుంచుకోవాలి లేదా సాహిత్యాన్ని చూడాలి. వాస్తవానికి, మీరు ఏ మార్పును చూడకపోయినా కొంత మొత్తంలో అణువులు కరిగిపోతాయి, కాబట్టి ప్రయోగం ఖచ్చితమైనదిగా ఉండటానికి మీరు ఈ మొత్తంలో ద్రావణాన్ని ఎలా లెక్కించాలో తెలుసుకోవాలి.
దశలు
2 యొక్క పద్ధతి 1: శీఘ్ర నియమాలను ఉపయోగించండి
అయానిక్ సమ్మేళనాల గురించి తెలుసుకోండి. ప్రతి అణువు సాధారణంగా నిర్దిష్ట సంఖ్యలో ఎలక్ట్రాన్లను కలిగి ఉంటుంది, కానీ కొన్నిసార్లు అది ఎలక్ట్రాన్ను పొందుతుంది లేదా ఇస్తుంది. ఈ ప్రక్రియ దీన్ని ఒకటి చేస్తుంది అయాన్లు వసూలు చేయబడింది. ప్రతికూల చార్జ్ (ఒక ఎలక్ట్రాన్ కంటే ఎక్కువ) ఉన్న అయాన్ సానుకూల చార్జ్తో (ఎలక్ట్రాన్ లేదు) అయాన్ను ఎదుర్కొన్నప్పుడు, అవి రెండు అయస్కాంతాల కాథోడ్ మరియు యానోడ్ లాగా కలిసిపోతాయి. ఫలితం అయానిక్ సమ్మేళనాన్ని ఏర్పరుస్తుంది.
- అయాన్లకు నెగటివ్ చార్జ్ అని పిలుస్తారు అయాన్లు, మరియు అయాన్లు సానుకూల చార్జ్ అని పిలువబడతాయి కేషన్.
- సాధారణంగా ఒక అణువులోని ఎలక్ట్రాన్ల సంఖ్య ప్రోటాన్ల సంఖ్యకు సమానం, కాబట్టి దీనికి ఛార్జ్ ఉండదు.
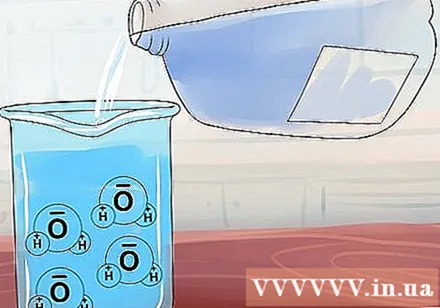
ద్రావణీయతను అర్థం చేసుకోండి. నీటి అణువు (H.2O) ఒక క్రమరహిత నిర్మాణాన్ని కలిగి ఉంది, కనుక ఇది అయస్కాంతాన్ని పోలి ఉంటుంది: ఒక చివర సానుకూల చార్జ్ కలిగి ఉంటుంది మరియు మరొకటి ప్రతికూల చార్జ్ కలిగి ఉంటుంది. మీరు నీటిలో ఒక అయానిక్ సమ్మేళనాన్ని ఉంచినప్పుడు, ఈ నీటి "అయస్కాంతాలు" దాని చుట్టూ సేకరించి, సానుకూల మరియు ప్రతికూల అయాన్లను వేరుగా లాగడానికి ప్రయత్నిస్తాయి.- కొన్ని అయానిక్ సమ్మేళనాలు చాలా గట్టిగా గ్రహించబడవు, అవి పరిగణించబడతాయి కరిగే ఎందుకంటే ఇది నీటిలో కలిపినప్పుడు విడిపోయి కరిగిపోతుంది. ఇతర సమ్మేళనాలు బలమైన బంధాలను కలిగి ఉంటాయి కరగని ఎందుకంటే నీటి అణువు యొక్క ఆకర్షణతో సంబంధం లేకుండా అయాన్లు ఒకదానికొకటి గట్టిగా ఆకర్షించబడతాయి.
- కొన్ని సమ్మేళనాలు నీటి అణువు యొక్క ఆకర్షణకు సమానమైన బంధన శక్తిని కలిగి ఉంటాయి. వాటిని పరిగణిస్తారు కొద్దిగా కరిగేది ఎందుకంటే చాలా సమ్మేళనాలు వేరు చేయబడతాయి, కాని మిగిలినవి ఒకదానికొకటి ఆకర్షించబడతాయి.
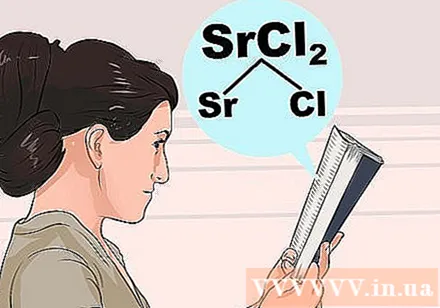
రద్దు సూత్రాన్ని అర్థం చేసుకోండి. అణువుల మధ్య పరస్పర చర్యలు చాలా క్లిష్టంగా ఉన్నందున, ఏ సమ్మేళనాలు చేయగలవు లేదా చేయలేదో వేరు చేయడానికి మీరు పూర్తిగా అంతర్ దృష్టిపై ఆధారపడలేరు. దాని సాధారణ లక్షణాల కోసం దిగువ జాబితాలోని సమ్మేళనం లోని మొదటి అయాన్ను చూడండి, ఆపై రెండవ అయాన్ దానితో అసాధారణంగా సంకర్షణ చెందకుండా చూసుకోండి.- ఉదాహరణకు, స్ట్రోంటియం క్లోరైడ్ (SrCl2), దయచేసి దిగువ బోల్డ్ దశల్లో Sr లేదా Cl కోసం చూడండి. Cl "సాధారణంగా కరిగేది" కాబట్టి దాని క్రింద ఉన్న మినహాయింపుల కోసం తనిఖీ చేయండి. Sr మినహాయింపు జాబితాలో లేదు కాబట్టి SrCl2 కరిగేదిగా ఉండాలి.
- ప్రతి నియమానికి అత్యంత సాధారణ మినహాయింపులు నియమం క్రింద వ్రాయబడ్డాయి. ఇతర మినహాయింపులు ఉన్నాయి, అయితే ఇవి సాధారణ కెమిస్ట్రీ లేదా ల్యాబ్ గంటలలో సంభవించే అవకాశం లేదు.
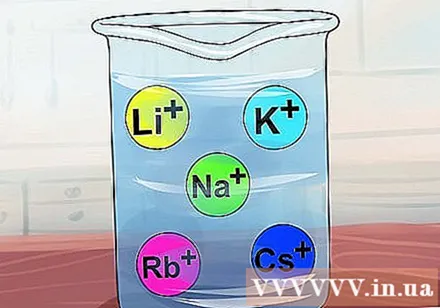
లి, నా, కె, ఆర్బి మరియు సిఎస్ వంటి క్షార లోహాలను కలిగి ఉన్నప్పుడు సమ్మేళనాలు కరుగుతాయి. ఈ లోహాలను గ్రూప్ IA ఎలిమెంట్స్ అని కూడా పిలుస్తారు: లిథియం, సోడియం, పొటాషియం, రుబిడియం మరియు సీసియం. ఈ అయాన్లలో ఒకదానిని కలిగి ఉన్న దాదాపు అన్ని సమ్మేళనాలు కరిగేవి.- మినహాయింపు: లి3పిఒ4 విడదీయరానిది.
సమ్మేళనాలు లేవు3, సి2హెచ్3ఓ2, లేదు2, ClO3 మరియు ClO4 అన్నీ కరిగేవి. పై అయాన్లకు సంబంధించిన పేర్లు నైట్రేట్, అసిటేట్, నైట్రేట్, క్లోరేట్ మరియు పెర్క్లోరేట్. అసిటేట్ తరచుగా OAc గా సంక్షిప్తీకరించబడిందని గమనించండి.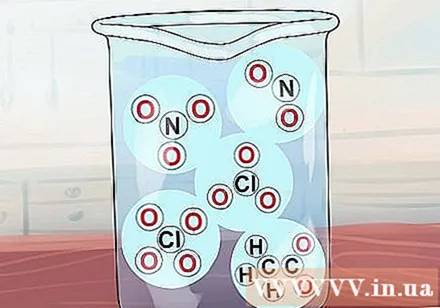
- మినహాయింపు: Ag (OAc) (సిల్వర్ అసిటేట్) మరియు Hg (OAc)2 (పాదరసం అసిటేట్) కరగనిది.
- ఆగ్నో2 మరియు KClO4 "కొద్దిగా కరిగించినవి" మాత్రమే.
Cl, Br మరియు I యొక్క సమ్మేళనాలు సాధారణంగా కరిగేవి. క్లోరైడ్, బ్రోమైడ్ మరియు అయోడైడ్ అయాన్లు దాదాపు ఎల్లప్పుడూ కరిగే సమ్మేళనాలను ఏర్పరుస్తాయి, వీటిని హాలోజన్ లవణాలు అంటారు.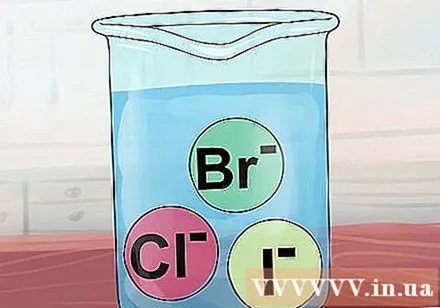
- మినహాయింపు: పై అయాన్లలో ఏదైనా వెండి అయాన్లతో కలిస్తే, పాదరసం Hg2, లేదా పిబి సీసం, కరగని సమ్మేళనాలను ఏర్పరుస్తుంది. రాగి Cu మరియు థాలి Tl తో కలిపినప్పుడు ఏర్పడిన తక్కువ సాధారణ సమ్మేళనాలకు కూడా ఇది వర్తిస్తుంది.
SO కలిగి ఉన్న సమ్మేళనాలు4 సాధారణంగా కరిగేది. సల్ఫేట్ అయాన్లు తరచుగా కరిగే సమ్మేళనాలను ఏర్పరుస్తాయి, అయితే చాలా మినహాయింపులు ఉన్నాయి.
- మినహాయింపు: సల్ఫేట్ అయాన్లు కింది అయాన్లతో కరగని సమ్మేళనాన్ని ఏర్పరుస్తాయి: స్ట్రోంటియం ఎస్ఆర్, బేరియం బా, సీసం పిబి, సిల్వర్ ఎగ్, కాల్షియం సి, రేడియం రా, మరియు సిల్వర్ మోనాటమ్ ఎగ్2. సిల్వర్ సల్ఫేట్ మరియు కాల్షియం సల్ఫేట్ మధ్యస్తంగా మాత్రమే కరిగేవని గమనించండి, కాబట్టి కొంతమంది వాటిని కొద్దిగా కరిగేదిగా భావిస్తారు.
OH లేదా S కలిగిన పదార్థాలు కరగవు. ఈ అయాన్ల సంబంధిత పేర్లు హైడ్రాక్సైడ్లు మరియు సల్ఫైడ్లు.
- మినహాయింపు: మీకు క్షార లోహాలు (గుంపులు I-A) గుర్తుందా మరియు అవి కరిగే సమ్మేళనాలను ఎలా ఏర్పరుస్తాయి? లి, నా, కె, ఆర్బి మరియు సిస్ అన్నీ హైడ్రాక్సైడ్ లేదా సల్ఫైడ్ అయాన్లతో కరిగే సమ్మేళనాలను ఏర్పరుస్తాయి. అదనంగా, హైడ్రాక్సైడ్లు ఆల్కలీన్ ఎర్త్ మెటల్ అయాన్లతో (గ్రూప్ II-A) కరిగే లవణాలను ఏర్పరుస్తాయి: కాల్షియం Ca, స్ట్రోంటియం Sr మరియు బేరియం బా. గమనిక: హైడ్రాక్సైడ్లు మరియు ఆల్కలీన్ ఎర్త్ లోహాలతో తయారైన సమ్మేళనాలు వాస్తవానికి గణనీయమైన సంఖ్యలో అణువులను కలిగి ఉంటాయి, కాబట్టి అవి కొన్నిసార్లు "కొద్దిగా కరిగేవి" గా పరిగణించబడతాయి.
CO- కలిగిన సమ్మేళనాలు3 లేదా PO4 విడదీయరానిది. కార్బోనేట్ మరియు ఫాస్ఫేట్ అయాన్ల కోసం చివరిసారిగా తనిఖీ చేయండి మరియు మీ సమ్మేళనం కరిగేదా అని మీరు చూస్తారు.
- మినహాయింపు: ఈ అయాన్లు లి, నా, కె, ఆర్బి మరియు సిఎస్ వంటి క్షార లోహాలతో పాటు అమ్మోనియం అయాన్ ఎన్హెచ్ తో కరిగే సమ్మేళనాలను ఏర్పరుస్తాయి.4.
2 యొక్క పద్ధతి 2: స్థిరమైన K నుండి కరిగే సామర్థ్యాన్ని లెక్కించండిsp
కరిగే ఉత్పత్తి స్థిరాంకం K ను చూడండిsp. ప్రతి సమ్మేళనం కోసం ఈ స్థిరాంకం భిన్నంగా ఉంటుంది, కాబట్టి మీరు దీన్ని పాఠ్యపుస్తకంలో లేదా ఆన్లైన్లోని గ్రాఫ్లో చూడాలి. ఈ విలువలు ప్రయోగాత్మకంగా నిర్ణయించబడతాయి మరియు గ్రాఫ్ల మధ్య గణనీయంగా మారవచ్చు కాబట్టి, అందుబాటులో ఉంటే పాఠ్య పుస్తకం యొక్క గ్రాఫ్ను ఉపయోగించడం మంచిది. పేర్కొనకపోతే, చాలా ప్లాట్లు 25ºC యొక్క పరీక్ష ఉష్ణోగ్రతని ume హిస్తాయి.
- ఉదాహరణకు, మీరు పిబిఐ ఫార్ములాతో సీసం అయోడైడ్ను కరిగించారని అనుకుందాం2, దాని ద్రావణీయత ఉత్పత్తి స్థిరాంకం రాయండి. మీరు bilbo.chm.uri.edu వద్ద గ్రాఫ్ను సూచిస్తే, మీరు స్థిరమైన 7,1 × 10 ను ఉపయోగిస్తారు.
రసాయన సమీకరణాన్ని వ్రాయండి. మొదటిది, కరిగినప్పుడు ఈ సమ్మేళనం యొక్క అయానిక్ విభజన నమూనాను నిర్ణయించండి. అప్పుడు K తో సమీకరణం రాయండిsp ఒక వైపు మరియు భాగం అయాన్లు మరొక వైపు.
- ఉదాహరణకు, ఒక PbI అణువు2 Pb, I మరియు I అయాన్లుగా విడదీయండి. (మీరు అన్ని అయాన్ల విద్యుత్తు తటస్థంగా ఉన్నందున మీరు అయాన్ యొక్క ఛార్జ్ను మాత్రమే తెలుసుకోవాలి లేదా తనిఖీ చేయాలి).
- 7,1 × 10 = సమీకరణాన్ని వ్రాయండి
- ఈ సమీకరణం ద్రావణీయ స్థిరాంకం, మీరు ద్రావణీయ పటంలో 2 అయాన్ల కోసం తెలుసుకోవచ్చు. 2 l- అయాన్లు ఉన్నందున, l- తప్పనిసరిగా చతురస్రాకారంగా ఉండాలి.
వేరియబుల్స్ ఉపయోగించడానికి సమీకరణాలను మార్చండి. అణువుల మరియు అయాన్ల సంఖ్య గురించి మీకు తెలిసిన సమాచారాన్ని ఉపయోగించి సాధారణ బీజగణిత పద్ధతులను ఉపయోగించి సమీకరణాన్ని తిరిగి వ్రాయండి. కరిగించడానికి సమ్మేళనం యొక్క ద్రవ్యరాశికి సమానంగా x ని సెట్ చేయండి మరియు x ప్రతి అయాన్ సంఖ్యను సూచించే సమీకరణాన్ని తిరిగి వ్రాస్తుంది.
- ఈ ఉదాహరణలో, మేము 7,1 × 10 = సమీకరణాన్ని తిరిగి వ్రాయాలి
- సమ్మేళనంలో ఒకే సీసం అయాన్ (పిబి) మాత్రమే ఉన్నందున, కరిగిన అణువుల సంఖ్య ఉచిత సీసం అయాన్ల సంఖ్యకు సమానం. అందువల్ల మనం దానిని x కు సెట్ చేయవచ్చు.
- ప్రతి సీసం అయాన్కు రెండు అయోడిన్ అయాన్లు (I) ఉన్నందున, మేము అయోడిన్ అణువుల సంఖ్యను 2x కి సమానంగా సెట్ చేస్తాము.
- ఇప్పుడు సమీకరణం 7.1 × 10 = (x) (2x) అవుతుంది
సాధారణ అయాన్లు ఏదైనా ఉంటే పరిగణనలోకి తీసుకోండి. మీరు స్వేదనజలంలో సమ్మేళనాన్ని కరిగించుకుంటే ఈ దశను దాటవేయండి. ఇప్పటికే ఒకటి లేదా అంతకంటే ఎక్కువ కాంపోనెంట్ అయాన్లు ("సాధారణ అయాన్లు") ఉన్న ద్రావణంలో ఒక సమ్మేళనం కరిగిపోతే, సమ్మేళనం యొక్క ద్రావణీయత గణనీయంగా తగ్గుతుంది. సాధారణ అయాన్ల ప్రభావం వాస్తవంగా కరగని సమ్మేళనాలపై చాలా స్పష్టంగా ఉంటుంది, మరియు ఈ సందర్భంలో సమతుల్యత వద్ద ఉన్న అయాన్లు చాలావరకు గతంలో ద్రావణంలో ఉన్నాయని మీరు అనుకోవచ్చు. ఇప్పటికే ద్రావణంలో ఉన్న అయాన్ల యొక్క మోలార్ ఏకాగ్రతను (లీటరుకు మోల్ లేదా M) లెక్కించడానికి సమీకరణాన్ని తిరిగి వ్రాయండి, ఈ విలువను ఆ అయాన్ కోసం మీరు ఉపయోగించే వేరియబుల్ x తో భర్తీ చేయండి.
- ఉదాహరణకు, సీసం అయోడైడ్ సమ్మేళనం 0.2M సీసం క్లోరైడ్ (PbCl) ద్రావణంలో కరిగిపోతే2), మేము సమీకరణాన్ని 7.1 × 10 = (0.2M + x) (2x) గా తిరిగి వ్రాస్తాము. X కంటే 0.2M అధిక సాంద్రత కనుక, మేము దానిని 7.1 × 10 = (0.2M) (2x) కు తిరిగి వ్రాయగలము.
సమీకరణాన్ని పరిష్కరించండి. X కోసం పరిష్కరించండి, మరియు మీరు సమ్మేళనం యొక్క ద్రావణీయతను చూస్తారు. ద్రావణీయ స్థిరాంకం యొక్క నిర్వచనంలో, మీరు మీ జవాబును లీటరు నీటికి కరిగించిన సమ్మేళనం యొక్క మోల్స్ సంఖ్య పరంగా వ్రాయాలి. తుది సమాధానం కనుగొనడానికి మీరు మీ కంప్యూటర్ను ఉపయోగించాల్సి ఉంటుంది.
- కింది ఉదాహరణ ఎటువంటి సాధారణ అయాన్లు లేకుండా స్వేదనజలంలో కరిగే సామర్థ్యం.
- 7.1 × 10 = (x) (2x)
- 7.1 × 10 = (x) (4x)
- 7.1 × 10 = 4x
- (7,1 × 10) 4 = x
- x = ∛ ((7,1 × 10) 4)
- x = లీటరుకు 1,2 x 10 మోల్స్ కరిగిపోతాయి. ఇది చాలా చిన్న ద్రవ్యరాశి, కాబట్టి ఈ సమ్మేళనం దాదాపు కరగదు.
నీకు కావాల్సింది ఏంటి
- సమ్మేళనం యొక్క కరిగే ఉత్పత్తి స్థిరాంకాల పట్టిక (K.sp)
సలహా
- కరిగిన సమ్మేళనాల మొత్తంపై మీకు ప్రయోగాత్మక డేటా ఉంటే, మీరు కరిగే స్థిరాంకం K కోసం పరిష్కరించడానికి అదే సమీకరణాన్ని ఉపయోగించవచ్చు.sp.
హెచ్చరిక
- ఈ నిబంధనల నిర్వచనాలపై ఏకాభిప్రాయం లేదు, కాని రసాయన శాస్త్రవేత్తలు మెజారిటీ సమ్మేళనాలను అంగీకరిస్తున్నారు. కరిగే మరియు కరగని అణువులు గణనీయమైన భాగాలను కలిగి ఉన్న అనేక ప్రత్యేక సమ్మేళనాలు, వీటిలో ప్రతి సమ్మేళనాల యొక్క విభిన్న వర్ణన ఉంటుంది.
- కొన్ని పాత పాఠ్యపుస్తకాలు NH ను చూస్తాయి4OH ఒక కరిగే సమ్మేళనం. ఇది నిజం కాదు; చిన్న మొత్తంలో NH అయాన్లు కనుగొనబడ్డాయి4 మరియు OH కానీ ఈ రెండు అయాన్లు సమ్మేళనాలలో కలిసిపోలేవు.